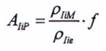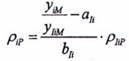TIÊU CHUẨN QUỐC GIA TCVN 13676:2023 (ISO 21676:2018) VỀ CHẤT LƯỢNG NƯỚC – XÁC ĐỊNH PHẦN HÒA TAN CỦA MỘT SỐ THÀNH PHẦN DƯỢC HOẠT TÍNH, SẢN PHẨM CHUYỂN HÓA VÀ CÁC CHẤT HỮU CƠ KHÁC TRONG NƯỚC VÀ NƯỚC THẢI ĐÃ QUA XỬ LÝ – PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO – KHỐI PHỔ (HPLC-MS/MS HOẶC -HRMS) SAU KHI BƠM TRỰC TIẾP
TCVN 13676:2023
ISO 21676:2018
CHẤT LƯỢNG NƯỚC – XÁC ĐỊNH PHẦN HÒA TAN CỦA MỘT SỐ THÀNH PHẦN DƯỢC HOẠT TÍNH, SẢN PHẨM CHUYỂN HÓA VÀ CÁC CHẤT HỮU CƠ KHÁC TRONG NƯỚC VÀ NƯỚC THẢI ĐÃ QUA XỬ LÝ – PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO – KHỐI PHỔ (HPLC – MS/MS HOẶC – HRMS) SAU KHI BƠM TRỰC TIẾP
Water quality- Determination of the dissolved fraction of selected active pharmaceutical
ingredients, transformation products and other organic substances in water and treated waste
water – Method using high performance liquid chromatography and mass spectrometric
detection (HPLC-MS/MS or-HRMS) after direct injection
Lời nói đầu
TCVN 13676:2023 hoàn toàn tương đương với ISO 21676:2018.
TCVN 13676:2023 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC 147 Chất lượng nước biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
Lời giới thiệu
Các thành phần dược phẩm là cần thiết cho sức khoẻ con người và động vật. Thông qua việc sử dụng hoặc thải bỏ không đúng cách, các thành phần dược hoạt tính đi vào chu trình nước không bị thay đổi hoặc biến đổi. Điều này có thể xảy ra đối với nước thải đô thị. Bởi vậy, một số thành phần dược hoạt tính và các sản phẩm chuyển hóa không bị loại bỏ hoàn toàn khỏi nước thải bằng kỹ thuật xử lý thông thường. Các thành phần dược hoạt tính và các sản phẩm chuyển hóa của chúng cũng đi qua bùn vào đất và sau đó đi vào các vùng nước qua nước rỉ rác, tùy thuộc vào bản chất của mặt đất và các thành phần hoạt tính. Các thành phần dược hoạt tính và các sản phẩm chuyển hóa của chúng, do đỏ, được tìm thấy trong nước thải đã qua xử lý, cũng như trong nước mặt và nước ngầm. Tiêu chuẩn này quy định phương pháp sắc ký lỏng cùng với đo khối phổ để xác định các thành phần dược hoạt tính được chọn và các sản phẩm chuyển hóa của chúng trong phần hòa tan.
CHẤT LƯỢNG NƯỚC – XÁC ĐỊNH PHẦN HÒA TAN CỦA MỘT SỐ THÀNH PHẦN DƯỢC HOẠT TÍNH, SẢN PHẨM CHUYỂN HÓA VÀ CÁC CHẤT HỮU CƠ KHÁC TRONG NƯỚC VÀ NƯỚC THẢI ĐÃ QUA XỬ LÝ – PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO – KHỐI PHỔ (HPLC – MS/MS HOẶC – HRMS) SAU KHI BƠM TRỰC TIẾP
Water quality- Determination of the dissolved fraction of selected active pharmaceutical
ingredients, transformation products and other organic substances in water and treated waste water – Method using high performance liquid chromatography and mass spectrometric detection (HPLC-MS/MS or-HRMS) after direct injection
CẢNH BÁO – Người sử dụng tiêu chuẩn này cần phải thành thạo với các thực hành trong phòng thí nghiệm thông thường. Tiêu chuẩn này không đề cập tới mọi vấn đề an toàn đối với người sử dụng tiêu chuẩn, nếu có. Người sử dụng có trách nhiệm xây dựng biện pháp bảo đảm an toàn và sức khỏe.
QUAN TRỌNG – Điều cần thiết là các thử nghiệm được tiến hành theo tiêu chuẩn này phải được thực hiện bởi nhân viên có trình độ phù hợp.
Tiêu chuẩn này quy định phương pháp xác định phần hòa tan của các thành phần dược hoạt tính được chọn và các sản phẩm chuyển hóa, cũng như các chất hữu cơ khác (xem Bảng 1) trong nước uống, nước ngầm, nước mặt và nước thải đã qua xử lý.
Phạm vi áp dụng dưới của phương pháp có thể thay đổi tùy thuộc vào độ nhạy của thiết bị được sử dụng và nền mẫu. Đối với hầu hết các hợp chất áp dụng tiêu chuẩn này, phạm vi áp dụng > 0,025 μg/L đối với nước uống, nước ngầm và nước mặt và > 0,050 μg/L đối với nước thải đã qua xử lý.
Phương pháp này có thể được sử dụng để xác định các chất hữu cơ khác hoặc trong các loại nước khác (ví dụ như nước quá trình) với điều kiện là độ chính xác đã được thử và kiểm tra xác nhận cho từng trường hợp và các điều kiện bảo quản của cả mẫu lẫn dung dịch chuẩn đã được xác nhận giá trị sử dụng. Bảng 1 đưa ra các chất đã được xác định bằng phương pháp này. Bảng E.1 đưa ra các ví dụ về việc xác định các chất hữu cơ khác.
Bảng 1 – Các chất được xác định theo tiêu chuẩn này
|
Tên thường gọi Tên hóa chất (IUPACa) |
Công thức phân tử |
Khối lượng phân tử g/mol |
CAS-RNb |
| 4-Axetylaminoantipyrin
N-(2,3-Dimetyl-5-oxo-1-phenyl-3-pyrazolin-4-yl)axetamin |
C13H15N3O2 |
245,28 |
83-15-8 |
| N4-Axetyl sulfamethoxazol
N-{4-[(5-Metyl-t,2-oxazol-3-yl)sulfamoyl]phenyl}-axetamin |
C12H13N3O4S |
295,32 |
21312-10-7 |
| Axit diatrizoic (axit amidotricoic)
axit 3,5-Bis(axetamido)-2,4,6-triiodobenzoic |
C11H9l3N2O4 |
613,91 |
117-96-4 |
| Atenolol
(RS)-2-[4-[2-Hydroxy-3-(1-metyletylamino) propoxylphenyl] etanamin |
C14H22N2O3 |
266,34 |
29122-68-7 |
| Bezafibrat
axit 2-{4-[2-(4-Clobenzamido)etyl]phenoxyl}-2-metylpropanoic |
C19H20CINO4 |
361,80 |
41859-67-0 |
| Bisoprolol
(RS]-l-[4-(2-lsopropoxyethoxymetyl]phenoxy]-3-isopropylamino-2-propanol |
C18H31NO4 |
325,45 |
66722-44-9 |
| Carbamazepin
5H-Dibenzo[b,f]azepin-5-carbamin |
C15H12N2O |
236,27 |
298-46-4 |
| Clarithromycin
(2R,3R,4S,5R,8R,9S,10S,11R,12R,14R)-11-[(2S,3R,4S,6R)-4- (dimetylamino]-3-hydroxy-6-metyloxan-2-yl]oxy-5-etyl-3,4-dihydroxy-9- [(2R,4R,5S,6S]-5-hydroxy-4-methoxy-4,6-dimetyl-oxan-2-yl]oxy-12- methoxy-2,4,8,10,12,14-hexa-metyl-6-oxacyclotetradecan-1,7-dione |
C38H69NO13 |
747,95 |
81103-11-9 |
| Axit clofibric
Axti 2-(4-Clophenoxy)-2-metylpropanoic |
C10H11CIO3 |
214,70 |
882-09-7 |
| Dehydrato-Erythromycin (anhydro-erythromycin)
(2R,3R,4S,5S,8R,9S,10S,11R,12R)-11-{[4-(dimetylamino)-3-hy-droxy-6- metyloxan-2-yl]oxy}-5-etyl-3-hydroxy-9-[(5-hydroxy-4-methoxy-4,6- dimetyloxan-2-yl)oxy]-2,4,8,10,12,14-hexame-ty I-6,15,16- trioxatricyclo[10.2.1.1{1,4}]hexadecan-7-one |
C37H65NO12 |
715,91 |
23893-13-2 |
| Diazepam
(RS)-7-Clo-1-metyl-5-phenyl-1,3-dihydro-2H-1,4-benzodiazepin-2-one |
C16H13CIN2O |
284,74 |
439-14-5 |
| Diclofenac
axit 2-[2-[(2,6-Diclophenyl)amino]phenyl]axetic |
C14H11CI2NO2 |
296,15 |
15307-86-5 |
| a IUPAC: Liên minh quốc tế về hoá học cơ bản và hoá học ứng dụng.
b CAS-RN: Số đăng ký hoá chất. |
|||
Bảng 1 – (tiếp theo)
|
Tên thường gọi Tên hóa chất (IUPACa) |
Công thức phân tử |
Khối lượng phân từ g/mol |
CAS-RNb |
| 10,11 -Dihydro-10,11-dihydroxy carbamazepin (5S,6S)-5,6-Dihydroxy-5,6-dihydrobenzo[b][1]benzazepie-11-carboxamin |
C15H14N2O3 |
270,29 |
58955-93-4 |
| Erythromycin
6-(4-Dimety lamino-3-hydroxy-6-metyl-oxan-2-yl]oxy-14-ety I-7,12,13 trihydroxy-4-(5-hyđroxy-4-methoxy-4,6-dimetyl-oxan-2-yl)-oxy- 3,5,7,9,11,13-hexametyl-1-oxacyclo-tetradecan-2,10-dione |
C37H67NO13 |
733,93 |
114-07-8 |
| 4-Formylaminoantipyrin
N-(2,3-Dihydro-1,5-dimetyl-3-oxo-2-phenyl-1H-pyrazol-4-yl) formamin |
C12H13N3O2 |
231,25 |
1672-58-8 |
| Gemfibrozil
axit 5-(2,5-clophenoxy)-2,2-mety Ipropanoic |
C15H22O3 |
250,34 |
25812-30-0 |
| Ibuprofen
axit (RS)-2-[4-(2-Metylpropyl)phenyl]propanoic |
C13H18O2 |
206,28 |
15687-27-1 |
| lomeprol
(+)-N,N’-Bis-(2,3-dihydroxypropyl)-5-[(2-hydroxy-axetyl]metylamino]-2,4,6- triiodo isophtalamin |
C17H22I3N3O8 |
777,09 |
78649-41-9 |
| lopamidol
(S)-N, N’-Bis[2-hydroxy-1 -(hydroxy mety l)etyl]-5-[(2-hy- droxypropanoyl)amino]-2,4,6-triiodobenzen-1,3-dicarbamin |
C17H22I3N3O3 |
777,08 |
60166-93-0 |
| lopromin
(±)-N,N’-Bis(2,3-dihydroxypropyl)-2,4,6-triiodo-5-(2-methoxyaxetamido)-N–metylisophtalamin |
C18H24I3N3O8 |
791,12 |
73334-07-3 |
| Metoprolol
(RS)-1-(lsopropylamino)-3-[4-(2-methoxyetyl) phenoxy] propan-2-ol |
C15H25NO3 |
267,36 |
37350-58-6 |
| Naproxen
axit (S)-2-(6-Methoxy-2-naphtyl)propanoic |
C14H14O3 |
230,26 |
22204-53-1 |
| Oxazepam
(RS)-7-Clo-3-hydroxy-5-phenyl-1,3-dihydro-2H-1,4-benzodiazepin-2-on |
C15H11CIN2O2 |
286,71 |
604-75-1 |
| Phenazon
1,5-Dimetyl-2-phenyl-2,3-dihydro-1 H-pyrazol-3-on |
C11H12N2O |
188,23 |
60-80-0 |
| Primidon
5-Etyl-5-phenylhexahydropyrimidin-4,6-dione |
C12H14N2O2 |
218,25 |
125-33-7 |
| a IUPAC: Liên minh quốc tế về hoá học cơ bản và hoá học ứng dụng.
b CAS-RN: Số đăng ký hoá chất. |
|||
Bảng 1 – (kết thúc)
|
Tên thường gọi Tên hóa chất (IUPACa) |
Công thức phân tử |
Khối lượng phân từ g/mol |
CAS-RNb |
| Propyphenazon
1,5-Dimetyl-4-(1-metyletyl)-2-phenyl-1,2-dihydro-3H-pyrazol-3-one |
C14H18N2O |
230,31 |
479-92-5 |
| Roxithromycin
(3R,4S,5S,6R,7R,9R,11S,12R,13S,14R)-6-{[(2S,3R,4S,6R)-4- (dimetylamino)-3-hydroxy-6-metyloxan-2-yl]oxy}-14-etyl-7,12,13-trihydroxy- 4-{[C2R,4R,5S,6S)-5-hy-droxy-4-methoxy-4,6-dimetyloxan-2-yl]oxy}- 3,5,7,9,11,13-hexametyl-10-(2,4,7-trioxa-1-azaoctan-1-yliden)-1- oxacyclotetradecan-2-one |
C41H76N2O15 |
837,05 |
80214-83-1 |
| Sotalol
(RS)-4′-(1 -Hydroxy-2-isopropylaminoetyl) metansulfonanilid |
C12H20N2O3S |
272,36 |
3930-20-9 |
| Sulfamethoxazol
4-Amino-N-(5-metyl-1,2-oxazol-3-yl]benzene-sulfonamin |
C10H11N3O3S |
253,28 |
723-46-6 |
| Temazepam
(RS)-7-Clo-3-hydroxy-1 -metyl-5-phenyl-1,3-dihydro-2H-1,4-benzodiazepin- 2-one |
C16H13CIN2O2 |
300,74 |
846-50-4 |
| Trimethoprim
2,4-Diamino-5-(3,4,5-trimethoxybenzyl)pyrimidin |
C14H18N4O3 |
290,32 |
738-70-5 |
| a IUPAC: Liên minh quốc tế về hoá học cơ bản và hoá học ứng dụng.
b CAS-RN: Số đăng ký hoá chất. |
|||
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4581 (ISO 3696), Nước dùng trong phòng thí nghiệm phân tích – Yêu cầu kỹ thuật và phương pháp thử
TCVN 6661-1 (ISO 8466-1), Chất lượng nước – Hiệu chuẩn và đánh giá các phương pháp phân tích và ước lượng các đặc trưng thống kê – Phần 1: Đánh giá thống kê các hàm chuẩn tuyến tính
TCVN 6663-4 (ISO 5667-4), Chất lượng nước – Lấy mẫu – Phần 4: Hướng dẫn lấy mẫu từ hồ, tự nhiên và nhân tạo
TCVN 6663-5 (ISO 5667-5), Chất lượng nước – Lấy mẫu – Phần 5: Hướng dẫn lấy mẫu nước uống từ các công trình xử lý và hệ thống phân phối đường ống
TCVN 6663-6 (ISO 5667-6), Chất lượng nước – Lấy mẫu – Phần 6: Hướng dẫn lấy mẫu sông và suối
TCVN 6663-10 (ISO 5667-10), Chất lượng nước – Lấy mẫu – Phần 10: Hướng dẫn lấy mẫu nước thải
TCVN 6663-11 (ISO 5667-11), Chất lượng nước – Lấy mẫu – Phần 11: Hướng dẫn lấy mẫu nước ngầm
TCVN7153 (ISO 1042), Dụng cụ thí nghiệm bằng thủy tinh – Bình định mức
TCVN 9561-2 (ISO 4796-2), Dụng cụ thí nghiệm bằng thủy tinh – Chai – Phần 2: Chai cổ côn
Trong tiêu chuẩn này không quy định các thuật ngữ và định nghĩa.
Mẫu nước được bơm trực tiếp vào hệ thống phân tích. Việc hhận dạng (đjnh tính) và định lượng được thực hiện bằng cách sử dụng sắc ký lỏng hiệu năng cao kết hợp với detector khối phổ (HPLC-MS/MS, HPLC-HRMS).
5.1 Trong quá trình chuẩn bị mẫu
Việc thất thoát chất phân tích có thể xảy ra trong quá trình lọc mẫu do hấp phụ.
5.2 Trong quá trình chạy sắc ký lỏng hiệu năng cao – khối phổ
Việc kéo đuôi pic, pic xảy ra phía trước và/hoặc pic kéo rộng là các chỉ thị về HPLC bị trục trặc và/hoặc có các cản trở xảy ra trong quá trình sắc ký. Tuy nhiên, có một số hợp chất có xu hướng hiển thị nhiều tín hiệu kéo đuôi hơn các hợp chất khác tùy thuộc vào các điều kiện sắc ký.
Sự cản trở từ các chất đi kèm (nền mẫu) có thể xảy ra ở cả chế độ ion hóa dương và âm phụ thuộc vào hợp chất cần đo (ví dụ: diclofenac ở chế độ ESI âm).
Các chất đi kèm (nền mẫu) có thể ảnh hưởng đến sự ion hóa của các chất cần xác định (ví dụ: ức chế ion hoặc tăng tín hiệu). Điều này có thể dẫn đến đánh giá thấp hoặc đánh giá quá cao nồng độ trong khi xác định. Những cản trở này có thể được phát hiện và hiệu chỉnh, khi cần, bằng cách sử dụng độ thu hồi chất phân tích (11.2 và Phụ lục B) và/hoặc chất chuẩn nội (10.3 và Bảng D.3).
Nếu sẵn có, cần sử dụng các thuốc thử tinh khiết “để phân tích” hoặc “để phân tích dư lượng”. Lượng tạp chất có trong giá trị mẫu trắng hoặc gây nhiễu tín hiệu phải không đáng kể. Việc này phải được kiềm tra thường xuyên (xem 9.5).
Dung môi, nước và thuốc thử dùng làm chất rửa giải phải tương thích với HPLC và đo khối phổ.
CHÚ THÍCH: Các loại dung môi có độ tinh khiết cao có bản sẵn trên thị trường.
6.1.1 Nước, phù hợp với các yêu cầu của TCVN 4581 (ISO 3696), loại 1 hoặc loại tương đương mà không có bất kỳ giá trị mẫu trắng làm cản trở.
6.1.2 Metanol, CH3OH.
6.1.3 Axetonitril, CH3CN.
6.1.4 Axit axetic, w(CH3COOH) = 100 % theo khối lượng.
6.1.5 Axit formic, w(HCOOH) không nhỏ hơn 98 % theo khối lượng.
6.1.6 Amoni axetat, w(CH3COONH4) không nhỏ hơn 99 % theo khối lượng.
6.1.7 Amoni format, w(HCOONH4) không nhỏ hơn 99 % theo khối lượng.
6.1.8 Natri thiosunfat pentahydrat, Na2S2O3.5H2O.
6.1.9 Các khí vận hành cho máy khối phổ, phù hợp với các thông số kỹ thuật của nhà sản xuất thiết bị.
6.1.10 Chất chuẩn, được liệt kê trong Bảng 1, đã biết theo khối lượng.
6.1.11 Chất chuẩn nội, tốt nhất là dùng các hợp chất chuẩn được đánh dấu đồng vị (xem Bảng D.3).
Các chất chuẩn nội không được làm cản trở chất phân tích (xem 9.5).
6.2.1 Yêu cầu chung
Các dung dịch chất chuẩn nội là cần thiết chỉ khi hiệu chuẩn và đánh giá đã tiến hành theo 10.3 và 12.3.
Kiểm tra độ chính xác của các dung dịch chất chuẩn dựa vào chuẩn kiểm soát (xem 6.2.9), ví dụ trong quá trình hiệu chuẩn (xem 10.1).
CHÚ THÍCH: Dung dịch chất chuẩn và chất chuẩn nội có sẵn trên thị trường.
6.2.2 Dung dịch gốc (chất chuẩn/chất chuẩn nội)
Chuẩn bị các dung dịch có nồng độ khối lượng, ví dụ: 0,1 mg/mL mỗi chất.
Trong trường hợp ví dụ trên, sử dụng một lượng 5 mg chất (6.1.10) trong các bình định mức 50 mL (7.2) riêng biệt. Hòa tan chúng trong axetonitril (6.1.3) hoặc metanol (6.1.2), sau đó thêm dung môi vào dung dịch cho đến vạch.
CHÚ THÍCH: Cách khác, có thể sử dụng các dung dịch gốc của các chất chuẩn riêng lẻ (hoặc các chất chuẩn nội) trong dung môi hữu cơ có bán sẵn để chuẩn bị các dung dịch pha loãng tiếp theo.
Bảo quản dung dịch ở nhiệt độ dưới -15 °C và tránh ánh sáng và bay hơi. Trong điều kiện này, dung dịch này ổn định trong một năm.
6.2.3 Dung dịch pha loãng trung gian A (chất chuẩn)
Chuẩn bị dung dịch trung gian có nồng độ khối lượng, ví dụ, 1 μg/mL của mỗi chất.
Việc này bao gồm: ví dụ, 0,5 mL từng dung dịch gốc chất chuẩn (xem 6.2.2) vào bình định mức 50 mL (7.2) và sau đó thêm axetonitril (6.1.3) đến vạch.
Bảo quản dung dịch ở nhiệt độ dưới -15 °C và tránh ánh sáng và bay hơi. Trong điều kiện này, dung dịch có thể ổn định trong một năm.
6.2.4 Dung dịch pha loãng trung gian B (chất chuẩn)
Chuẩn bị dung dịch trung gian có nồng độ khối lượng, ví dụ, 50 ng/mL của mỗi chất.
Việc này bao gồm: ví dụ, chuyển 0,5 mL dung dịch pha loãng trung gian A (xem 6.2.3) vào bình định mức 10 mL (7.2) và sau đó loãng bằng nước (6.1.1) đến vạch.
Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C và tránh ánh sáng và bay hơi. Trong điều kiện này, dung dịch có thể ổn định trong một tháng.
Sử dụng dung dịch này để thêm chất phân tích vào mẫu để xác định độ thu hồi (xem 11.2).
6.2.5 Dung dịch pha loãng trung gian C (chất chuẩn)
Chuẩn bị dung dịch trung gian có nồng độ khối lượng, ví dụ: 5 ng/mL của mỗi chất.
Việc này bao gồm: ví dụ, chuyển 0,25 mL dung dịch pha loãng trung gian A (xem 6.2.3) vào bình định mức 50 mL (7.2) và sau đó pha loãng bằng nước (6.1.1) đến vạch.
Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C và tránh ánh sáng và tránh bay hơi. Trong điều kiện này, dung dịch có thể ổn định trong một tháng.
6.2.6 Dung dịch pha loãng trung gian D (chất chuẩn nội)
Chuẩn bị dung dịch trung gian có nồng độ khối lượng, ví dụ: 1 μg/mL của mỗi chất.
Việc này bao gồm: ví dụ, chuyển 0,5 mL từng dung dịch gốc chất chuẩn nội (xem 6.2.2) vào bình định mức 50 mL (7.2) và thêm axetonitrìl (6.1.3) đến vạch.
Bảo quản dung dịch ở nhiệt độ dưới -15 °C và tránh ánh sáng và bay hơi. Trong điều kiện này, dung dịch có thể ổn định trong một năm.
6.2.7 Dung dịch pha loãng trung gian E (chất chuẩn nội)
Chuẩn bị dung dịch trung gian có nồng độ khối lượng, ví dụ, 50 ng/mL của mỗi chất.
Việc này bao gồm: ví dụ, chuyển 0,5 mL dung dịch pha loãng trung gian D (xem 6.2.6) vào bình định mức 10 mL (7.2) và thêm nước (6.1.1) đến vạch.
Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C và tránh ánh sáng và bay hơi. Trong điều kiện này, dung dịch có thể ổn định trong một tháng.
Sử dụng dung dịch này để có được các mẫu hiệu chuẩn và các mẫu thêm chuẩn.
6.2.8 Mẫu hiệu chuẩn
Chuẩn bị các mẫu hiệu chuẩn từ các dung dịch pha loãng tương ứng của dung dịch pha loãng trung gian C (xem 6.2.5). Để hiệu chuẩn bằng chất chuẩn nội (xem 10.3), sử dụng cùng lượng chất chuẩn nội cho từng mẫu hiệu chuẩn.
Chuẩn bị các mẫu hiệu chuẩn, ví dụ các dung dịch có nồng độ khối lượng của các chất cần xác định tương ứng với 0,025 μg/L và nồng độ của các chất chuẩn nội tương ứng với 0,250 μg/L (xem 10.1).
Ví dụ, chuyền 50 μL dung dịch pha loãng trung gian C (xem 6.2.5) vào bình định mức 10 mL, trộn 50 μL dung dịch pha loãng trung gian E (xem 6.2.7) và sau đó thêm nước (6.1.1) đến vạch.
Nếu có thể, thành phần của các mẫu hiệu chuẩn phải giống với thành phần của các mẫu được kiểm tra và không dẫn đến việc mở rộng pic gây cản trở. Khi sử dụng các mẫu hiệu chuẩn trong nước uống, nước ngầm hoặc nước mặt, phải đảm bảo không có mặt các chất cần xác định.
CHÚ THÍCH: Khi các mẫu hiệu chuẩn được chuẩn bị trong nước siêu tinh khiết, điều này có thể dẫn đến kết quả macroli tthấp hơn. Trong những trường hợp này, việc sử dụng nước siêu tinh khiết không được ưu tiên mà cần hiệu chuẩn phù hợp với nền mẫu.
Chuẩn bị các mẫu hiệu chuẩn mới cho mỗi trình tự đo mới nếu không thể kiểm tra xác nhận được độ ổn định của chúng.
6.2.9 Chuẩn kiểm soát
Chuẩn kiểm soát là dung dịch chất chuẩn được tạo ra độc lập với các dung dịch gốc, ví dụ: dung dịch từ một mẻ hoặc từ nhà sản xuất. Dung dịch này cần chứa tất cả các chất cần xác định.
Thiết bị hoặc các bộ phận của thiết bị tiếp xúc với mẫu nước không được ảnh hưởng đến các hợp chất cần đo. Tất cả các thiết bị được sử dụng tốt nhất là được làm bằng thủy tinh, thép không gỉ hoặc polytetrafluoroetylen (PTFE).
7.1 Chai có đáy phẳng và cổ hẹp, tốt nhất là loại có khớp nối hình côn thủy tinh màu nâu với nút thủy tinh, ví dụ: chai phòng thí nghiệm, dung tích 250 mL phù hợp với TCVN 9561-2 (ISO 4796-2) – NS 250.
7.2 Bình định mức, dung tích danh nghĩa 10 mL, 25 mL, 50 mL, ví dụ bình định mức phù hợp với TCVN 7153 (ISO 1042)-A50-C.
7.3 Microxyranh.
7.4 Bộ lọc bằng xyranh, có thể tích chết thấp, ví dụ đường kính 13 mm có màng xenlulo tái tạo.
Việc lọc không được làm thất thoát đáng kể các chất riêng lẻ và bộ lọc phải được chọn bằng cách kiểm tra điều này. Cần kiểm tra xác nhận không bị nhiễm hoặc thất thoát đáng kể chất cần phân tích từ quá trình lọc bằng cách dùng các mẫu trắng và dung dịch chất chuẩn cho đi qua cùng bộ lọc.
7.5 Lọ đựng mẫu (vial), thích hợp với bộ bơm mẫu tự động, ví dụ: dung tích danh nghĩa 1,5 mL với nắp và setum bằng cao SU/PTFE.
CHÚ THÍCH: Có thể sử dụng bổ sung lọ mẫu bằng polyetylen (PE) để giảm thiểu thất thoát macrolit.
7.6 Cột HPLC, tốt nhất là dùng tiền cột, thích hợp cho sắc ký của các chất đã chọn. Xem Phụ lục C để biết các ví dụ.
7.7 Máy sắc ký lỏng hiệu năng cao, cùng với máy đo khối phổ, bao gồm các bộ phận sau.
7.7.1 Bộ loại khí, ví dụ: bộ khử khí chân không.
7.7.2 Hệ thống bơm phân tích, có xung thấp, thích hợp cho rửa giải gradient nhị phân.
7.7.3 Bộ bơm mẫu thủ công hoặc tự động.
7.7.4 Thiết bị kiểm soát ổn nhiệt của cột tách, ví dụ bộ ổn nhiệt cột.
7.7.5 Detector khối phổ (MS/MS, HRMS), tốt nhất là với ion hóa tia điện (ESI).
Lấy mẫu theo các quy định trong TCVN 6663-4 (ISO 5667-4), TCVN 6663-5 (ISO 5667-5), TCVN 6663-6 (ISO 5667-6), TCVN 6663-10 (ISO 5667-10) và TCVN 6663-11 (ISO 5667-11).
Sử dụng các chai có đáy phẳng (7.1) để lấy mẫu và đổ đầy mẫu nước cần kiểm tra vào các chai.
Khi lấy nước uống có thể chứa các chất oxy hóa, thêm vào mỗi lít khoảng 50 mg natri thiosulfat pentahydrat (6.1.8).
Phân tích mẫu nước càng sớm càng tốt sau khi lấy mẫu.
Bảo quản mẫu ở nhiệt độ (3 ± 2) °C, tránh ánh sáng, tối đa ba tuần.
CHÚ THÍCH: Nếu cần bảo quản lâu hơn và/hoặc trong trường hợp nghi ngờ hoặc đã xác nhận giá trị sử dụng có sự không ổn định của các chất riêng lẻ, thì có thể thực hiện các biện pháp thích hợp (ví dụ bảo quản bằng cách đông lạnh mẫu).
9.1 Yêu cầu chung
Việc thực hiện phương pháp phụ thuộc vào loại hiệu chuẩn và các biện pháp dự kiến đề nhận dạng và hiệu chính các hiệu ứng nền, nếu cần.
9.2 Chuẩn bị mẫu
Nếu mẫu không nhìn thấy rõ các hạt thì lọc mẫu qua bộ lọc bằng xyranh (7.4).
Trong quá trình lọc mẫu, quá trình hấp phụ có thể làm hao hụt chất phân tích, đặc biệt là các chất kị nước (ví dụ: macrolit). Trong trường hợp này, không lọc mẫu trước khi sắc ký mà sử dụng bộ lọc dòng thay thế để bảo vệ cột tách khỏi các hạt.
Khi hiệu chuẩn bằng chất chuẩn ngoại (xem 10.2), thu lấy một phần mẫu để xác định độ thu hồi, nếu cần (xem 11.2).
Khi hiệu chuẩn bằng chất chuẩn nội (xem 10.3), thì bổ sung chất chuẩn nội sao cho nồng độ khối lượng của chất chuẩn nội trong mẫu bằng với nồng độ khối lượng của chất chuẩn nội trong mẫu hiệu chuẩn (xem 6.2.8).
Cần tính đến độ loãng của mẫu do thêm thuốc thử khi tính các kết quả riêng lẻ (xem 12.2) nếu tổng thể tích lớn hơn 1 %.
Theo dõi rửa giải sớm, ví dụ: metformin (xem Bảng E.1), về thời gian lưu và hình dạng pic. Mức dung môi hữu cơ trong mẫu đã chuẩn bị không được làm rộng pic bổ sung.
9.3 Sắc ký lỏng hiệu năng cao (HPLC)
Vận hành thiết bị HPLC theo hướng dẫn của nhà sản xuất.
Sử dụng cột HPLC (7.6) thích hợp để tách sắc ký và tối ưu hóa việc tách các chất phân tích bằng rửa giải gradient.
Chọn các điều kiện sắc ký để thu được độ nhạy tối ưu cho việc phát hiện khối phổ (xem Phụ lục C về các ví dụ).
CHÚ THÍCH 1: Việc sử dụng chương trình gradient với axetonitril/nước/axit axetic có lợi về độ nhạy đối với hầu hết các chất.
CHÚ THÍCH 2: Ở cùng tốc độ dòng rửa giải tuyến tính, cột có đường kính trong nhỏ hơn thể hiện độ nhạy tốt hơn cột có đường kính lớn hơn.
Việc tách hoàn toàn các chất là không cần thiết với điều kiện không xảy ra nhiễu của phép định lượng trong quá trình chồng pic.
Thời gian lưu ngắn nhất phải tương ứng với tối thiểu ba lần thời gian của thể tích chết của cột HPLC.
Sử dụng sắc ký để tách các chất không thể tách hoàn toàn ra khỏi nhau bằng phương pháp đo phổ. Trong những trường hợp này, độ phân giải sắc ký R nhỏ nhất phải = 1,2.
Chọn thể tích bơm thích hợp để không xảy ra hiện tượng mở rộng pic gây nhiễu hoặc làm cản trở phép định lượng.
CHÚ THÍCH 3: Đối với thể tích bơm lớn hơn, ví dụ: 1 mL, kỹ thuật chuyển cột với các cột làm giàu thích hợp có thể thực hiện được nhưng nằm ngoài phạm vi của phương pháp này.
Kiểm tra độ lệch chuẩn thời gian lưu một lần trong quá trình đánh giá ban đầu. Độ lệch chuẩn thời gian lưu không được quá 0,03 min đối với sáu sắc ký đồ liên tiếp.
9.4 Phát hiện
9.4.1 Yêu cầu chung
Vận hành thiết bị đo khối phổ theo hướng dẫn của nhà sản xuất và chọn cài đặt chính xác cho thiết bị.
Chế độ ESI thường được ưu tiên khi ion hóa các chất. Điều này thường tạo ra các ion bán phân tử kiểu [M+H]+ hoặc [M-H]–. Trong các trường hợp riêng biệt, các ion cộng, ví dụ [M+ NH4]+ hoặc [M+Na]+, cũng có thể được tạo thành trong các điều kiện sắc ký nhất định.
Hầu hết các chất được liệt kê trong Bảng 1 có thể được phát hiện bằng cách sử dụng chế độ ESI dương. Các chất được phát hiện ở chế độ ESI âm có thể được phân tích trong một lần chạy bằng cách đổi cực hoặc thử nghiệm trong một làn chạy riêng (xem Bảng D.1).
Khi thực hiện phát hiện đồng thời các ion âm và dương, chọn thời gian đổi cực đủ ngắn để bảo toàn đủ số lượng điểm dữ liệu.
Từng pic phải được bảo đảm bằng 8 điểm dữ liệu.
Nhận dạng và cài đặt theo phương pháp cụ thể về các thông số nguồn và thông số MS sử dụng các chất ít nhạy hơn, ví dụ: ibuprofen.
CHÚ THÍCH: Tín hiệu thường được làm rõ trước khi tích phân pic. Tùy thuộc vào thuật toán được sử dụng mà có thể làm mất cường độ tín hiệu cao không tương xứng khi số lượng điểm dữ liệu quá thấp. Khả năng tái lập của tích phân pic cũng có thể bị ảnh hưởng, đặc biệt là đối với các giá trị chiều cao và điện tích pic thấp nếu có quá ít điểm dữ liệu.
Sử dụng sắc ký để tách các chất không thể tách hoàn toàn khỏi nhau bằng phương pháp khối phổ (xem 9.3).
9.4.2 Phép đo hai lần khối phổ (MS/MS)
Nhận dạng việc thiết lập tối ưu cho quá trình ion hóa trong các điều kiện sắc ký quy định cho từng chất ở chế độ ion dương hoặc âm phụ thuộc vào tính chất hóa học của chất.
Chọn cài đặt cho chất cụ thể để có thể bảo toàn hai ion sản phẩm cho mỗi chất, nếu có thể. Tối ưu hóa sự chuyển khối thứ hai liên quan đến khối lượng đồng vị, ví dụ, 37CI (xem Bảng D.1) đối với các chất phân mảnh chỉ thành một ion sản phẩm được phát hiện, nếu có thể. Trong những trường hợp này, để tránh nhiễu trong quá trình định lượng, chỉ sử dụng chất chuẩn nội có khối lượng mol tương đối cao hơn khối lượng mol của chất cần xác định ít nhất bốn đơn vị khối lượng. Các ví dụ được nêu trong Bảng D.3.
9.4.3 Phép đo khối phổ có độ phân giải cao (HRMS)
Khi sử dụng thiết bị khối phổ có độ phân giải cao ở chế độ quét toàn bộ, phổ khối lượng hoàn chỉnh là có sẵn tại mỗi thời điểm trong quá trình chạy sắc ký.
Đảm bảo và kiểm tra độ chính xác khối lượng (xem 12.1) và độ phân giải được duy trì trên toàn bộ diện tích khối lượng và toàn bộ sắc ký đồ.
Chọn độ phân giải để thu được đủ sự khác biệt của các tín hiệu nền mẫu.
Cài đặt phương pháp đo sao cho đối với mỗi chất phân tích thu được ít nhất một ion sản phẩm đề xác nhận (xem 12.1), nếu có thể.
Khi chọn các chất chuẩn được đánh dấu đồng vị, đảm bảo rằng sự chênh lệch khối lượng của các chất phân tích không được đánh dấu tối thiểu là ba đơn vị khối lượng để tránh bất kỳ sự cản trở nào đối với tín hiệu đồng vị của chất phân tích. Các ví dụ được đưa ra trong Bảng D.3.
9.5 Đo giá trị mẫu trắng
Thường xuyên thực hiện các phép đo giá trị mẫu trắng đối với phương pháp hoàn chỉnh để kiểm tra không có cản trở từ thiết bị, dụng cụ hoặc thuốc thử.
Ví dụ, bơm nước (6.1.1) để thực hiện phép đo giá trị mẫu trắng.
Nếu các giá trị mẫu trắng có gây cản trở (trên 50 % mức báo cáo thấp nhất), thì xác định nguyên nhân, sử dụng phương pháp kiểm tra hệ thống và loại bỏ các nguồn ô nhiễm.
Việc hiệu chuẩn phương pháp xác định phải được thực hiện trong các điều kiện sắc ký quy định. Thời gian lưu của các chất phân tích riêng lẻ và của các chất chuẩn nội phải được xác định trước. Chúng có thể được xác định bằng cách bơm hỗn hợp nhiều thành phần hoặc các dung dịch của các chất riêng lẻ sử dụng khối lượng của các ion sản phẩm hoặc các ion bán phân tử trong điều kiện sắc ký quy định.
Tiến hành như sau:
– Thiết kế phương pháp xác định hoàn chỉnh để tạo ra mối quan hệ tuyến tính giữa tín hiệu đo được và nồng độ đối với từng chất cần xác định.
– Để thực hiện điều này, xác định dải làm việc tuyến tính của thiết bị bằng cách bơm ít nhất năm mẫu hiệu chuẩn (xem 6.2.8) với nồng độ khác nhau cho từng chất cần xác định [xem TCVN 6661-1 (ISO 8466-1)].
– Chọn dải hiệu chuẩn tuyến tính bao trùm các nồng độ thực tế, ví dụ: dải hiệu chuẩn từ 0,025 μg/L đến 1 μg/L để kiểm tra nước uống, nước ngầm và nước mặt.
– Mức nồng độ thấp nhất trong dải hiệu chuẩn phải cao hơn hoặc bằng giới hạn định lượng. Việc xác định giới hạn phát hiện và giới hạn định lượng được thực hiện theo các phương pháp đã được lập thành văn bản, ví dụ: phù hợp với TCVN 6661-1 (ISO 8466-1).
– Đối với hoạt động thường xuyên, chỉ cần thực hiện hiệu chuẩn ít nhất ba mức nồng độ là đủ.
– Đối với hiệu chuẩn nhiều điểm, phân bố đều các mức nồng độ trên dài hiệu chuẩn và thực hiện hiệu chuẩn theo TCVN 6661-1 (ISO 8466-1).
– Giữ thể tích bơm không đổi để hiệu chuẩn và đo mẫu.
Hàm hiệu chuẩn được xác định cho một chất cụ thể chỉ có giá trị đối với dải nồng độ áp dụng. Nó cũng phụ thuộc vào trạng thái hoạt động của hệ thống đp và phải được thử nghiệm trong từng dãy đo.
Hai quy trình được mô tả để thiết lập các hàm hiệu chuẩn:
a) hiệu chuẩn bằng chuẩn ngoại;
b) hiệu chuẩn bằng chuẩn nội.
Hiệu chuẩn với chất chuẩn nội được ưu tiên và rất khuyến khích khi có sẵn các chuẩn được đánh dấu.
Khi kiểm tra nước uống, nước ngầm và nước mặt, việc hiệu chuẩn với chất chuẩn ngoại (xem 10.2) sẽ dẫn đến kết quả không sai lệch quá 25 % so với giá trị thực của chúng đối với hầu hết các chất trong Bảng 1 mà không cần hiệu chính theo độ thu hồi. Có thể có ngoại lệ, đặc biệt là với các chất phân cực có thời gian lưu thấp, ví dụ: một số chất cản quang tia X, mà độ lệch hệ thống cao hơn có thể xảy ra do hiệu ứng nền. Trong những trường hợp này, có thể cần sử dụng chất chuẩn nội (xem 10.3) hoặc hiệu chính với độ thu hồi theo mẫu cụ thể (xem 11.2).
Hiệu ứng nền mẫu có thể xuất hiện, đặc biệt là trong các mẫu nước thải đã xử lý và gây cản trở trong suốt quá trình sắc ký tiếp theo đối với phép định lượng do sự triệt tiêu hoặc tăng ion. Hiệu ứng nền có thể được giảm bớt bằng cách pha loãng mẫu.
CHÚ THÍCH 1: Việc thực hiện hiệu chính sử dụng độ thu hồi mẫu cụ thể (xem 11.2) và sử dụng chất chuẩn nội (xem 10.3) đều làm tăng sai lệch độ không đảm bảo đo. Việc hiệu chính cũng có thể dẫn đến các giá trị cao giả. Để khẳng định kết quả định lượng, có thể áp dụng phương pháp thêm chuẩn với một số bước thêm chuẩn.
Hiệu ứng nền mẫu có thể phụ thuộc vào điều kiện làm việc hoặc kiểu loại và tình trạng của thiết bị và phải được xác định, ví dụ: bằng cách xác định độ thu hồi, khi áp dụng phương pháp cho các loại mẫu quan tâm. Nếu có thể, thành phần của các mẫu hiệu chuẩn (xem 6.2.8) phải giống với thành phần của các mẫu cần kiểm tra.
CHÚ THÍCH 2: Hiệu ứng nền cũng có thể được phát hiện thông qua việc khuếch tán sau cột các chất phân tích hoặc chất chuẩn nội trong thời gian sắc ký hoàn chỉnh mẫu thực dựa trên sự giảm cường độ.
Bảng 2 giải thích các ký hiệu được sử dụng trong các công thức và nội dung sau đây.
Bảng 2 – Giải thích các ký hiệu
|
Ký hiệu |
Ý nghĩa |
|
i |
Nhận dạng của một chất |
|
j |
Con số liên tiếp đối với các cặp giá trị |
|
e |
Các biến đo lường để hiệu chuẩn |
|
a |
Các biến đo lường để bổ sung |
|
I |
Chuẩn nội |
|
M |
Dung dịch đo |
|
p |
Mẫu |
|
A |
Bổ sung |
10.2 Hiệu chuẩn bằng chất chuẩn ngoại
Bơm các mẫu hiệu chuẩn (xem 6.2.8) để thực hiện hiệu chuẩn.
Lập đồ thị biểu đồ hàm hiệu chuẩn. Để làm được điều này, dựng đồ thị các giá trị đo yie cho mỗi chất i trên trục y và nồng độ khối lượng tương ứng ρie trên trục X.
Xác định hàm chuẩn từ các cặp giá trị yie và ρie sử dụng hồi quy tuyến tính nêu trong Công thức (1):
|
yie = bi · ρie + ai |
(1) |
Trong đó:
yie là giá trị đo (biến phụ thuộc) của chất i trong quá trình hiệu chuẩn dưới dạng hàm của ρie, ví dụ đơn vị diện tích;
bi là độ dốc của hồi quy tuyến tính đối với chất i (tương ứng với hệ số đáp ứng cụ thể của chất), ví dụ: đơn vị diện tích * lít trên microgram (L/μg);
ρie là nồng độ khối lượng (biến độc lập) của chất i trong mẫu hiệu chuẩn, tính bằng microgam trên lít (μg/L);
ai là điểm chặn của hồi quy tuyến tính đối với chất i trên tọa độ, ví dụ: đơn vị diện tích.
10.3 Hiệu chuẩn bằng chất chuẩn nội
Việc sử dụng các chất chuẩn nội để phân tích định lượng có thể bù cho các cản trở có thể xảy ra trong quá trình đo khối phổ (xem Điều 5).
Chất chuẩn nội không được có mặt trong mẫu nước cần kiểm tra. Chất chuẩn nội này phải có những điểm tương đồng về mặt hóa học với chất cần xác định và phải hoạt động giống như chất cần xác định trong quá trình lọc, sắc ký và đo khối phổ.
Sử dụng các hợp chất làm chất chuẩn nội tương đương với các chất đang được khảo sát, có cấu trúc với các đồng vị khác nhau, ví dụ: các hợp chất được đánh dấu 13C hoặc đã detơri hóa (xem Bảng D.3).
Các chất phân tích không có hợp chất đánh dấu đồng vị có thể được đánh giá sử dụng các chất chuẩn nội khác, nếu điều này được đảm bảo thì ghi lại độ thu hồi của chất phân tích được tính từ việc bổ sung trong các loại mẫu được kiểm tra nằm trong cùng khoảng với độ thu hồi của chất chuẩn nội đã chọn.
Để thực hiện hiệu chuẩn, bơm các mẫu hiệu chuẩn (xem 6.2.8) có chứa tất cả các chất cần xác định cũng như các chất chuẩn nội (6.1.11).
Để hiển thị bằng đồ thị hàm hiệu chuẩn cho từng chất i, vẽ biểu đồ tỷ lệ của các giá trị đo được yie/yIie trên trục y và tỷ lệ nồng độ khối lượng ρie/ρIie tương ứng trên trục X.
Xác định hàm chuẩn từ các cặp giá trị yiej/yIiej và ρiej/ρIiej sử dụng hồi quy tuyến tính được cho trong Công thức (2):
|
|
(2) |
Trong đó:
yie xem Công thức (1):
yIie là giá trị đo được đối với chất chuẩn nội / của chất i trong quá trình hiệu chuẩn, ví dụ đơn vị diện tích;
ρie xem Công thức (1);
ρIie là nồng độ khối lượng của chất chuẩn nội / của chất i trong mẫu hiệu chuẩn, tính bằng microgam trên lít (μg/L);
bIi là độ dốc của hồi quy tuyến tính yie /yIie phụ thuộc vào tỷ lệ ρie/ρIie của chất i, không thứ nguyên;
aIi là điểm chặn của hồi quy tuyến tính trên tọa độ của chất i, ví dụ: đơn vị diện tích, không thứ nguyên.
11.1 Yêu cầu chung
Độ thu hồi chất phân tích có thể cung cấp các chỉ thị về ảnh hưởng của nền mẫu. Ví dụ, chúng có thể được xác định bằng cách tiến hành bổ sung vào mẫu như trong 11.2.
CHÚ THÍCH 1: Việc hiệu chính được thực hiện sử dụng độ thu hồi của mẫu cụ thể có thể dẫn đến độ không đảm bảo đo cao hơn.
Khi thực hiện hiệu chuẩn và đánh giá bằng chất chuẩn nội (xem 10.3 và 12.3), thì độ thu hồi của chất chuẩn nội là thước đo để đánh giá hiệu lực của phép phân tích trên thiết bị. Chúng phải được xác định theo 11.3.
Độ thu hồi chất phân tích của mẫu cụ thể hoặc độ thu hồi chất phân tích của chất chuẩn nội phải nằm trong khoảng từ 50 % đến 150 %.
CHÚ THÍCH 2: Độ thu hồi thấp dẫn đến giới hạn định lượng cao hơn và độ không đảm bảo đo cao hơn.
11.2 Tính độ thu hồi chất phân tích sử dụng mẫu
Để xác định độ thu hồi, thực hiện bổ sung chất phân tích trên mẫu, ví dụ: bằng cách thêm 50 μL dung dịch pha loãng trung gian B (xem 6.2.4) vào 5 mL mẫu và sau đó phân tích mẫu đã bổ sung và không bổ sung theo toàn bộ quá trình.
Lượng bổ sung phải nằm trong dải làm việc trung bình, ví dụ: 0,5 μg/L. Nồng độ khối lượng của chất phân tích được sử dụng trong các mẫu được bổ sung không được vượt quá dải hiệu chuẩn. Mẫu phải được pha loãng trước khi bổ sung, nếu cần.
Tính độ thu hồi AiP của chất i trong mẫu theo Công thức (3):
|
|
(3) |
Trong đó:
AiP là độ thu hồi của chất i trong mẫu, tính bằng phần trăm (%);
ρiaP là nồng độ khối lượng xác định của chất i trong mẫu có bổ sung chất phân tích, được tính theo Công thức (1), tính bằng microgam trên lít (μg/L);
ρi là nồng độ khối lượng xác định được của chất i trong mẫu không bổ sung chất phân tích, được tính theo Công thức (1), tính bằng microgam trên lít (μg/L);
ρiA là nồng độ khối lượng được bổ sung đối với chất i trong mẫu có bổ sung chất phân tích, tính bằng microgam trên lít (μg/L);
ƒ là hệ số chuyển đổi, trong trường hợp này ƒ =100, tính bằng phần trăm (%).
11.3 Độ thu hồi chất chuẩn nội
Tính độ thu hồi đối với các chất chuẩn nội theo Công thức (4):
|
|
(4) |
Trong đó:
AIiP là độ thu hồi đối với chất chuẩn nội I của chất i, tính bằng phần trăm (%);
ρIiM là nồng độ khối lượng xác định được đối với chất chuẩn nội I của chất i trong dung dịch đo, tính bằng microgam trên lít (μg/L);
ρIie xem Công thức (2);
ƒ xem Công thức (3).
12.1 Kiểm tra xác nhận các chất riêng rẽ
Khi sử dụng phương pháp HPLC MS/MS, chất có trong mẫu được coi là được kiểm tra xác nhận nếu:
a) trong sắc ký đồ MS/MS của vết khối lượng tạo ra bởi ion sản phẩm của chất này, thì tín hiệu nhận được có thời gian lưu tương ứng trong khoảng dung sai ±0,15 min so với thời gian lưu của chất chuẩn tương ứng, trong các điều kiện tiêu chuẩn, và
b) ion sản phẩm thứ hai từ cùng một ion mẹ hoặc từ một ion mẹ khác của chất này được phát hiện trên một vết khối lượng khác trong cùng thời gian lưu, và
c) cường độ của các ion sản phẩm có mối quan hệ với nhau tương ứng với tỷ lệ của các ion này được xác định theo chất chuẩn trong các điều kiện tiêu chuẩn với sai số ± 30 %. Dung sai này có thể đến 50 % tại giới hạn áp dụng dưới và đặc biệt là ở giới hạn định lượng đối với phương pháp phân tích này.
Khi sử dụng phương pháp HPLC-HRMS, chênh lệch khối lượng giữa khối lượng đo được và khối lượng lý thuyết của chất hoặc ion của chất này không được vượt quá 5 pμm1). Trong các điều kiện này, chất có trong mẫu được coi là đã được xác nhận nếu:
– trong sắc ký đồ HRMS của vết khối lượng được tạo ra bởi một ion bán phân tử (hoặc ion cộng) của chất, tín hiệu thu được với thời gian lưu tương ứng nằm trong dung sai ± 0,15 min với thời gian lưu được tạo ra bởi chất chuẩn tương ứng trong cùng điều kiện, và
– tín hiệu từ ít nhất một ion sản phẩm từ chất được phát hiện trong cùng một thời gian lưu.
CHÚ THÍCH: Phổ ion sản phẩm với khối lượng chính xác thường thu được khi áp dụng HRMS/MS.
Chất này cũng được coi là đã được kiểm tra xác nhận nếu, thay vì một ion sản phẩm từ chất được phát hiện trên sắc ký đồ HRMS, thì vết khối lượng của một đồng vị của ion bán phân tử, ví dụ: 37CI, 81Br, được phát hiện trong cùng một thời gian lưu và có tỷ lệ cường độ nằm trong dung sai ± 30 %. Dung sai này có thể lớn đến 50 % ở giới hạn áp dụng dưới và đặc biệt là ở giới hạn định lượng đối với phương pháp phân tích này.
Đối với các chất phân tích có cùng thời gian lưu và thành phần nguyên tố giống nhau, thì phải kiểm tra xác nhận sử dụng ion sản phẩm. Nếu các khối lượng này cũng giống nhau, thì cần phải tách sắc ký của các chất phân tích.
Nếu các tiêu chí kiểm tra xác nhận chỉ được đáp ứng một phần, ví dụ: chỉ với một ion sản phẩm có cường độ đủ trong phương pháp HPLC-MS/MS, nếu được chuyên gia đánh giá là cần thiết, có thể được hỗ trợ bằng cách:
– áp dụng kỹ thuật ion hóa khác có thể tạo ra các ion khác nhau, ví dụ: ESI âm hoặc APCI;
– thời gian lưu với cột HPLC có độ chọn lọc khác.
12.2 Tính kết quả riêng rẽ sử dụng hiệu chuẩn với chất chuẩn ngoại
Tính nồng độ khối lượng ρiP của chất i trong mẫu theo Công thức (5):
|
|
(5) |
Trong đó:
ρiP là nồng độ khối lượng của chất i trong mẫu, tính bằng microgam trên lít (μg/L);
yiM là giá trị đo được của chất i trong dung dịch được đo, ví dụ: đơn vị diện tích;
ƒ xem Công thức (3) (chỉ khi sử dụng độ thu hồi để tính toán);
ai, bi xem Công thức (1);
AiP xem Công thức (3) và 10.1 (chỉ khi sử dụng độ thu hồi để tính toán).
12.3 Tính các kết quả riêng lẻ sử dụng hiệu chuẩn với chất chuẩn nội
Tính nồng độ khối lượng ρiP của chất i trong mẫu theo Công thức (6):
|
|
(6) |
Trong đó:
ρiP xem Công thức (5);
yiM xem Công thức (5);
yIiM là giá trị đo được đối với chất chuẩn nội I của chất i trong dung dịch được đo, ví dụ: đơn vị diện tích;
ρIiP là nồng độ khối lượng đã xác định trước đối với chất chuẩn nội I của chất i trong mẫu, tính bằng microgam trên lít (μg/L);
aIi, bIi xem Công thức (2).
Kết quả phân tích thu được khi áp dụng tiêu chuẩn này phải tuân thủ độ không đảm bảo đo, xem ISO 11352[1], nghĩa là được xem xét khi giải thích kết quả (xem Phụ lục A).
Nồng độ khối lượng của các chất phù hợp với Bảng 1 được biểu thị bằng microgam trên lít với hai chữ số có nghĩa.
| VÍ DỤ: atenolol: | 0,091 μg/L |
| 0,15 μg/L | |
| 1,5 μg/L |
Báo cáo thử nghiệm phải bao gồm ít nhất các thông tin sau:
a) Phương pháp thử sử dụng, viện dẫn tiêu chuẩn này, ví dụ: TCVN 13676:2023 (ISO 21676:2018);
b) Nhận dạng mẫu;
c) Biểu thị kết quả phù hợp với Điều 13;
d) Tất cả các sai lệch so với phương pháp này;
e) Báo cáo về tất cả các trường hợp có thể ảnh hưởng đến kết quả.
Dữ liệu hiệu năng được đưa ra trong Bảng A.2 đến Bảng A.5 đã được xác định trong phép thử liên phòng để xác nhận giá trị sử dụng được thực hiện tại Đức từ ngày 13 tháng 1 năm 2014 đến ngày 31 tháng 1 năm 2014 bao gồm bốn mẫu (xem Bảng A.1), được bổ sung chất phân tích trong dải nồng độ từ 0,035 μg/L đến 0,90 μg/L. Một số chất cần định lượng đã có mặt trong các mẫu ban đầu. Các giá trị được ấn định dựa trên việc bổ sung chất phân tích và mức ô nhiễm ban đầu của các mẫu ban đầu được xác định trong nghiên cứu liên phòng. Trong số 18 phòng thí nghiệm tham gia, 16 phòng thí nghiệm sử dụng kỹ thuật hai lần khối phổ (MS/MS) và 2 phòng thí nghiệm sử dụng khối phổ có độ phân giải cao (HRMS), mỗi phòng đều không có bước lọc mẫu sơ bộ. Việc đánh giá được thực hiện theo TCVN 6910-2 (ISO 5725-2).
Bảng A.1 – Đặc trưng của các mẫu nghiên cứu liên phòng chưa được lọc
|
Thông số |
Đơn vị |
Nước uống (hai mẫu) |
Nước mặt |
Đầu ra của nhà máy xử lý nước thải |
| Giá trị pH |
– |
8,2 |
8,0 |
8,0 |
| TOC |
mg/L |
< 0,5 |
1,85 |
5,5 |
| Độ dẫn điện |
mS/m |
67 |
37 |
94 |
| Na |
mg/L |
35,8 |
24,1 |
106 |
| Ca |
mg/L |
85,8 |
39,8 |
69,1 |
Bảng A.2 đến Bảng A.5 đưa ra các dữ liệu hiệu năng.
Độ thu hồi cao đối với axit diatrizoic trong cả hai mẫu nước uống (Bảng A.2 và Bảng A.3) có thể được truy xuất trở lại mức ô nhiễm ban đầu trong nước uống ở mức xấp xỉ 0,06 μg/L.
Độ thu hồi cao và CV,R đối với các chất erythromycin, dehydrato-erythromycin, clarithromycin và roxithromycin có thể được truy xuất từ các kết quả từ các phòng thí nghiệm đã sử dụng các dung dịch hiệu chuẩn được chuẩn bị bằng nước siêu tinh khiết.
Bảng A.2 – Dữ liệu hiệu năng đối với nước uống trong phạm vi áp dụng dưới
|
Chất |
l |
n |
o % |
X μg/L |
μg/L |
η % |
SR μg/L |
CV,R % |
sr μg/L |
CV,r % |
| 4-Axetylaminoantipyrin |
13 |
49 |
7,5 |
0,0350 |
0,0308 |
87,9 |
0,0046 |
15,0 |
0,0013 |
4,1 |
| N4-Axetyl sulfamethoxazol |
16 |
61 |
0,0 |
0,0350 |
0,0345 |
98,6 |
0,0053 |
15 4 |
0,0022 |
6,4 |
| Axitdiatrizoic |
13 |
52 |
7,1 |
0,0350 |
0,0855 |
244,3 |
0,0245 |
28,7 |
0,0056 |
6,5 |
| Atenolol |
16 |
60 |
0,0 |
0,0350 |
0,0389 |
111,1 |
0,0067 |
17,2 |
0,0022 |
5,6 |
| Bezafibrat |
12 |
48 |
7,7 |
0,0350 |
0,0336 |
96,0 |
0,0035 |
10,4 |
0,0013 |
3,9 |
| Bisoprolol |
13 |
49 |
19,7 |
0,0350 |
0,0402 |
114,7 |
0 0047 |
11,8 |
0,0010 |
2,5 |
| Carbamazepin |
15 |
57 |
0,0 |
0,0350 |
0,0354 |
101,1 |
0,0055 |
15,4 |
0,0015 |
4,3 |
| Clarithromycin |
13 |
49 |
14,0 |
0,0350 |
0,0364 |
104,1 |
0,0090 |
24,6 |
0,0013 |
3,6 |
| Axit clofibric |
14 |
53 |
7,0 |
0,0350 |
0,0331 |
94,6 |
0,0042 |
12,8 |
0,0009 |
2,8 |
| Dehy drato-Ery th romyci n |
11 |
44 |
8,3 |
0,0350 |
0,0449 |
128,2 |
0,0151 |
33,6 |
0,0028 |
6,2 |
| Diazepam |
16 |
61 |
0,0 |
0,0350 |
0,0349 |
99,7 |
0,0039 |
11,2 |
0,0017 |
4,8 |
| Diclofenac |
14 |
53 |
7,0 |
0,0350 |
0,0362 |
103,4 |
0,0043 |
11,8 |
0,0017 |
4,7 |
| 10,11-Dihydro-10,11-dihydroxy carbamazepin |
13 |
49 |
14,0 |
0,0350 |
0,0333 |
95,1 |
0,0039 |
11,7 |
0,0019 |
5,6 |
| Erythromycin |
15 |
57 |
6,6 |
0,0350 |
0,0383 |
109,3 |
0,0103 |
26,8 |
0,0024 |
6,3 |
| 4-Formylaminoantipyrin |
16 |
60 |
0,0 |
0,0350 |
0,0353 |
100,9 |
0,0069 |
19,5 |
0,0016 |
4,6 |
| Gemfibrozil |
14 |
53 |
7,0 |
0,0350 |
0,0321 |
91,8 |
0,0034 |
10,5 |
0,0016 |
5,0 |
| Ibuprofen |
11 |
41 |
0,0 |
0,0350 |
0,0380 |
108,4 |
0,0085 |
22,5 |
0,0030 |
78 |
| lomeprol |
13 |
51 |
0,0 |
0,0350 |
0,0372 |
106,3 |
0,0084 |
22,6 |
0 0039 |
10,4 |
| lopamidol |
12 |
48 |
7,7 |
0,0350 |
0,0374 |
107,0 |
0,0064 |
17,2 |
0,0043 |
11,4 |
| lopromin |
14 |
56 |
6,7 |
0,0350 |
0,0376 |
107,3 |
0,0088 |
23,5 |
0,0028 |
7,5 |
| Metoprolol |
16 |
61 |
0,0 |
0,0350 |
0,0401 |
114,4 |
0,0046 |
11,6 |
0,0017 |
4,2 |
| Naproxen |
11 |
41 |
16,3 |
0,0350 |
0,0349 |
99,8 |
0,0061 |
17,3 |
0,0013 |
3,6 |
| Oxazepam |
14 |
53 |
13 1 |
0,0350 |
0,0339 |
96,7 |
0,0032 |
9,6 |
0,0015 |
4,3 |
| Phenazon |
16 |
61 |
0,0 |
0,0350 |
0,0356 |
101,7 |
0,0035 |
9,9 |
0,0017 |
4,9 |
| Primidon |
15 |
57 |
6,6 |
0,0350 |
0,0347 |
99,1 |
0,0034 |
9,7 |
0,0021 |
6,2 |
| Propyphenazon |
15 |
57 |
6,6 |
0,0350 |
0,0360 |
102,9 |
0,0033 |
9,2 |
0,0013 |
3.5 |
| Roxithromycin |
8 |
29 |
12,1 |
0,0350 |
0,0526 |
150,2 |
0,0220 |
41,8 |
0,0048 |
9,2 |
| Sotalol |
15 |
57 |
6,6 |
0,0350 |
0,0368 |
105,2 |
0,0051 |
13,8 |
0,0016 |
4,3 |
| Sulfamethoxazol |
12 |
48 |
14,3 |
0,0350 |
0,0335 |
95,6 |
0,0032 |
9,6 |
0,0014 |
4,3 |
| Temazepam |
12 |
45 |
21,1 |
0,0350 |
0,0338 |
96,5 |
0,0035 |
10,5 |
0,0010 |
2,8 |
| Trimethoprim |
16 |
61 |
0,0 |
0,0350 |
0,0378 |
107,9 |
0,0045 |
11,9 |
0,0018 |
4,7 |
| I là số phòng thí nghiệm sau khi loại bỏ ngoại lệ
n là số lượng các kết quả phân tích đơn lẻ sau khi loại bỏ ngoại lệ o là phần trăm ngoại lệ có liên quan X là giá trị nồng độ đúng (theo quy ước) của mẫu thử
η là tỷ lệ thu hồi sR là độ lệch chuẩn tái lập CV,R là hệ số biến thiên tái lập sr là độ lệch chuẩn lặp lại CV,r là hệ số biến thiên lặp lại |
||||||||||
Bảng A.3 – Dữ liệu hiệu năng đối với nước uống
|
Chất |
l |
n |
o % |
X μg/L |
μg/L |
η % |
SR μg/L |
CV,R % |
sr μg/L |
CV,r % |
| 4-Axetylaminoantipyrin |
16 |
60 |
1,6 |
0,0850 |
0,0715 |
84,2 |
0,0109 |
15,3 |
0,0029 |
4,0 |
| N4-Axetyl sulfamethoxazol |
16 |
61 |
0,0 |
0,0850 |
0,0826 |
97,2 |
0,0081 |
9,8 |
0,0039 |
4,7 |
| Axit diatrizoic |
15 |
57 |
0,0 |
0,0850 |
0,1541 |
181,2 |
0,0646 |
41,9 |
0,0084 |
5,5 |
| Atenolol |
15 |
57 |
6,6 |
0,0850 |
0,0927 |
109,0 |
0,0157 |
16,9 |
0,0029 |
3,2 |
| Bezafibrat |
16 |
61 |
0,0 |
0,0850 |
0,0793 |
93,3 |
0,0102 |
12,9 |
0,0035 |
4,4 |
| Bisoprolol |
14 |
53 |
13,1 |
0,0850 |
0,0955 |
112,4 |
0,0166 |
17,4 |
0,0024 |
2,6 |
| Carbamazepin |
14 |
53 |
13,1 |
0,0850 |
0,0872 |
102,6 |
0,0116 |
13,3 |
0,0020 |
2,3 |
| Clarithromycin |
16 |
61 |
0,0 |
0,0850 |
0,0940 |
110,6 |
0,0315 |
33,6 |
0,0055 |
5,8 |
| Axit clofibric |
14 |
53 |
13,1 |
0,0850 |
0,0832 |
97,8 |
0,0096 |
11,6 |
0,0018 |
2,2 |
| Dehydrato-Erythromycin |
13 |
52 |
7,1′ |
0,0850 |
0,0931 |
109,5 |
0,0274 |
29,4 |
0,0072 |
‘ 7,7 |
| Diazepam |
16 |
61 |
0,0 |
0,0850 |
0,0846 |
99,6 |
0,0106 |
12,6 |
0,0039 |
4,6 |
| Diclofenac |
15 |
57 |
6,6 |
0,0850 |
0,0887 |
104,3 |
0,0111 |
12,5 |
0,0027 |
3,1 |
| 10,11-Dihydro-10,11- dihydroxy carbamazepin |
15 |
57 |
0,0 |
0,0850 |
0,0810 |
95,3 |
0,0102 |
12,6 |
0,0043 |
5,3 |
| Erythromycin |
15 |
57 |
6,6 |
0,0850 |
0,0883 |
103,9 |
0,0246 |
27,9 |
0,0037 |
4,2 |
| 4-Formylaminoantipyrin |
13 |
49 |
19,7 |
0,0850 |
0,0860 |
101,1 |
0,0131 |
15,3 |
0,0022 |
2,6 |
| Gemfibrozil |
15 |
57 |
0,0 |
0,0850 |
0,0786 |
92,5 |
0,0088 |
11,2 |
0,0030 |
3,8 |
| Ibuprofen |
12 |
45 |
8,2 |
0,0850 |
0,0866 |
101,9 |
0,0112 |
13,0 |
0,0050 |
5,8 |
| lomeprol |
15 |
57 |
0,0 |
0,0850 |
0,0883 |
103,9 |
0,0160 |
18,1 |
0,0069 |
7,9 |
| lopamidol |
12 |
45 |
21,1 |
0,0850 |
0,0777 |
91,4 |
0,0110 |
14,1 |
0,0040 |
5,2 |
| lopromin |
14 |
53 |
13,1 |
0,0850 |
0,0843 |
99,1 |
0,0121 |
14,3 |
0,0063 |
7,4 |
| Metoprolol |
15 |
56 |
8,2 |
0,0850 |
0,0936 |
110,1 |
0,0098 |
10,4 |
0,0029 |
3,1 |
| Naproxen |
13 |
49 |
14,0 |
0,0850 |
0,0855 |
100,6 |
0,0127 |
14,9 |
0,0029 |
3,4 |
| Oxazepam |
13 |
49 |
19,7 |
0,0850 |
0,0821 |
96,6 |
0,0084 |
10,2 |
0,0020 |
2,5 |
| Phenazon |
16 |
61 |
0,0 |
0,0850 |
0,0858 |
100,9 |
0,0069 |
8,0 |
0,0033 |
3,9 |
| Primidon |
15 |
57 |
6,6 |
0,0850 |
0,0834 |
98,2 |
0,0097 |
11,7 |
0,0045 |
5,4 |
| Propyphenazon |
15 |
57 |
6,6 |
0,0850 |
0,0865 |
101,7 |
0,0056 |
6,5 |
0,0031 |
3,6 |
| Roxithromycin |
16 |
61 |
0,0 |
0,0850 |
0,0807 |
94,9 |
0,0428 |
53,1 |
0,0068 |
8,5 |
| Sotalol |
13 |
49 |
19,7 |
0,0850 |
0,0885 |
104,2 |
0,0089 |
10,0 |
0,0023 |
2,6 |
| Sulfamethoxazol |
15 |
57 |
6,6 |
0,0850 |
0,0801 |
94,3 |
0,0106 |
13,3 |
0,0038 |
4,8 |
| Temazepam |
15 |
57 |
0,0 |
0,0850 |
0,0804 |
94,6 |
0,0079 |
9,8 |
0,0043 |
5,4 |
| Trimethoprim |
13 |
49 |
19,7 |
0,0850 |
0,0889 |
104,6 |
0,0085 |
9,6 |
0,0027 |
3,0 |
| CHÚ THÍCH: Giải thích ký hiệu xem trong Bảng A.2 | ||||||||||
Bảng A.4 – Dữ liệu hiệu năng đối với nước mặt
|
Chất |
l |
n |
o % |
X Mg/L |
μg/L |
η % |
SR μg/L |
CV,R % |
sr Pg/L |
CV,r % |
| 4-Axetylaminoantipyrin |
14 |
53 |
13,1 |
0,317 |
0,300 |
94,6 |
0,0394 |
13,1 |
0,0063 |
2,1 |
| N4-Axetyl sulfamethoxazol |
16 |
61 |
0,0 |
0,125 |
0,128 |
102,4 |
0,0141 |
11,0 |
0,0046 |
3,6 |
| Axit diatrizoic |
15 |
57 |
0,0 |
0,253 |
0,260 |
102,8 |
0,0636 |
24,5 |
0,0140 |
5,4 |
| Atenolol |
15 |
57 |
6,6 |
0,125 |
0,144 |
115,2 |
0,0222 |
15,4 |
0,0061 |
4,2 |
| Bezafibrat |
16 |
61 |
0,0 |
0,157 |
0,147 |
93,6 |
0,0163 |
11,1 |
0,0032 |
2,1 |
| Bisoprolol |
16 |
61 |
0,0 |
0,155 |
0,164 |
105,8 |
0,0340 |
20,7 |
0,0046 |
2,8 |
| Carbamazepin |
12 |
45 |
26,2 |
0,179 |
0,180 |
100,6 |
0,0188 |
10,5 |
0,0029 |
1,6 |
| Clarithromycin |
15 |
57 |
6,6 |
0,125 |
0,163 |
130,4 |
0,0602 |
36,9 |
0,0062 |
3,8 |
| Axit clofibric |
12 |
45 |
26,2 |
0,125 |
0,120 |
96,0 |
0,0086 |
7,2 |
0,0018 |
1,5 |
| Dehydrato-Erythromycin |
14 |
56 |
0,0 |
0,125 |
0,166 |
132,8 |
0,0619 |
37,3 |
0,0116 |
7,0 |
| Diazepam |
15 |
57 |
6,6 |
0,125 |
0,121 |
96,8 |
0,0128 |
10,6 |
0,0025 |
2,1 |
| Diclofenac |
16 |
61 |
0,0 |
0,234 |
0,228 |
97,4 |
0,0233 |
10,2 |
0,0054 |
2,4 |
| 10,11-Dihydro-10,11- dihydroxy carbamazepin |
15 |
57 |
0,0 |
0,262 |
0,283 |
108,0 |
0,0988 |
34,9 |
0,0071 |
2,5 |
| Erythromycin |
14 |
53 |
13,1 |
0,125 |
0,146 |
116,8 |
0,0433 |
29,7 |
0,0056 |
3,8 |
| 4-Formylaminoantipyrin |
16 |
61 |
0,0 |
0,376 |
0,382 |
101,6 |
0,0611 |
16,0 |
0,0107 |
2,8 |
| Gemfibrozil |
15 |
57 |
0,0 |
0,125 |
0,117 |
93,6 |
0,0126 |
10,8 |
0,0034 |
2,9 |
| Ibuprofen |
11 |
41 |
16,3 |
0,125 |
0,128 |
102,4 |
0,0209 |
16,4 |
0,0048 |
3,7 |
| lomeprol |
15 |
57 |
0,0 |
0,360 |
0,391 |
108,6 |
0,0773 |
19,8 |
0,0233 |
6,0 |
| lopamidol |
15 |
57 |
0,0 |
0,297 |
0,296 |
99,7 |
0,0566 |
19,1 |
0,0149 |
5,1 |
| lopromin |
16 |
61 |
0,0 |
0,224 |
0,235 |
104,9 |
0,0335 |
14,2 |
0,0123 |
5,2 |
| Metoprolol |
15 |
57 |
6,6 |
0,288 |
0,292 |
101,4 |
0,0317 |
10,9 |
0,0075 |
2,6 |
| Naproxen |
15 |
57 |
0,0 |
0,125 |
0,139 |
111,2 |
0,0115 |
8,3 |
0,0060 |
4,3 |
| Oxazepam |
15 |
56 |
8,2 |
Ọ,125 |
0,138 |
110,4 |
0,0191 |
13,9 |
0,0039 |
2,8 |
| Phenazon |
15 |
57 |
6,6 |
0,125 |
0,125 |
100,0 |
0,0099 |
7,9 |
0,0026 |
2,1 |
| Primidon |
13 |
49 |
19,7 |
0,125 |
0,136 |
108,8 |
0,0148 |
10,9 |
0,0045 |
3,3 |
| Propyphenazon |
16 |
61 |
0,0 |
0,125 |
0,123 |
98,4 |
0,0103 |
8,3 |
0,0027 |
2,2 |
| Roxithromycin |
16 |
61 |
0,0 |
0,125 |
0,207 |
165,6 |
0,1370 |
66,2 |
0,0124 |
6,0 |
| Sotalol |
15 |
57 |
6,6 |
0,157 |
0,150 |
95,5 |
0,0145 |
9,6 |
0,0035 |
2,3 |
| Sulfamethoxazol |
14 |
53 |
13,1 |
0,155 |
0,137 |
88,4 |
0,0220 |
16,1 |
0,0027 |
2,0 |
| Temazepam |
14 |
53 |
7,0 |
0,125 |
0,116 |
92,8 |
0,0140 |
12,1 |
0,0042 |
3,6 |
| Trimethoprim |
16 |
61 |
0,0 |
0,125 |
0,134 |
107,2 |
0,0155 |
11,6 |
0,0039 |
2,9 |
| CHÚ THÍCH: Giải thích ký hiệu xem trong Bảng A.2 | ||||||||||
Bảng A.5 – Dữ liệu hiệu năng đối với nước thải đã xử lý
|
Chất |
l |
n |
o % |
X Mg/L |
μg/L |
η % |
SR μg/L |
CV,R % |
sr Pg/L |
CV,r % |
| 4-Axetylaminoantipyrin |
14 |
53 |
13,1 |
1,306 |
1,135 |
86,9 |
0,1873 |
16,5 |
0,0234 |
2,1 |
| N4-Axetyl sulfamethoxazol |
16 |
61 |
0,0 |
0,900 |
0,827 |
91,9 |
0,1329 |
16,1 |
0,0319 |
3,9 |
| Axit diatrizoic |
15 |
57 |
0,0 |
2,616 |
2,587 |
98,9 |
0,7031 |
27,2 |
0,1076 |
4,2 |
| Atenolol |
15 |
60 |
0,0 |
1,019 |
0,935 |
91,8 |
0,2371 |
25,3 |
0,0269 |
2,9 |
| Bezafibrat |
15 |
57 |
6,6 |
0,942 |
0,912 |
96,8 |
0,1184 |
13,0 |
0,0317 |
3,5 |
| Bisoprolol |
14 |
53 |
13,1 |
1,034 |
1,039 |
100,4 |
0,1313 |
12,6 |
0,0227 |
2,2 |
| Carbamazepin |
16 |
61 |
0,0 |
1,603 |
1,592 |
99,3 |
0,1746 |
11,0 |
0,0353 |
2,2 |
| Clarithromycin |
16 |
61 |
0,0 |
1,053 |
1,413 |
134,2 |
0,6310 |
44,7 |
0,0683 |
4,8 |
| Axit clofibric |
14 |
53 |
13,1 |
0,900 |
0,849 |
94,3 |
0,0973 |
11,5 |
0,0231 |
2,7 |
| Dehydrato-Erythromycin |
14 |
56 |
0,0 |
0,984 |
1,366 |
138,8 |
‘ 0,6036 |
44,2 |
0,0730 |
5,3 |
| Diazepam |
15 |
57 |
6,6 |
0,900 |
0,815 |
90,5 |
0,0973 |
11,9 |
0,0245 |
3,0 |
| Diclofenac |
14 |
53 |
13,1 |
2,221 |
2,228 |
100,3 |
0,1930 |
8,7 |
0,0379 |
1,7 |
| 10,11 -Dihydro-10,11 -dihydroxy carbamazepin |
14 |
53 |
7,0 |
2,090 |
1,968 |
94,2 |
0,3252 |
16,5 |
0,0653 |
3,3 |
| Erythromycin |
15 |
57 |
6,6 |
0,950 |
1,141 |
120,1 |
0,4150 |
36,4 |
0,0385 |
3,4 |
| 4-Formylaminoantipyrin |
14 |
53 |
13,1 |
1,445 |
1,439 |
99,6 |
0,1983 |
13,8 |
0,0285 |
2,0 |
| Gemfibrozil |
15 |
57 |
0,0 |
0,900 |
0,805 |
89,4 |
0,1690 |
21,0 |
0,0290 |
3,6 |
| Ibuprofen |
12 |
43 |
8,5 |
0,900 |
0,817 |
90,8 |
0,1776 |
21,7 |
0,0259 |
3,2 |
| lomeprol |
15 |
57 |
0,0 |
2,407 |
2,444 |
101,5 |
0,3687 |
15,1 |
0,1075 |
4,4 |
| lopamidol |
13 |
48 |
14,3 |
1,028 |
1,006 |
97,8 |
0,2011 |
20,0 |
0,0420 |
4,2 |
| lopromin |
15 |
56 |
0,0 |
3,759 |
3,739 |
99,5 |
0,5753 |
15,4 |
0,1209 |
3,2 |
| Metoprolol |
15 |
56 |
8,2 |
1,744 |
1,839 |
105,4 |
0,2330 |
12,7 |
0,0440 |
2,4 |
| Naproxen |
13 |
49 |
12,5 |
0,957 |
0,860 |
89,8 |
0,0772 |
9,0 |
0,0283 |
3,3 |
| Oxazepam |
15 |
56 |
8,2 |
0,995 |
0,918 |
92,3 |
0,1332 |
14,5 |
0,0293 |
3,2 |
| Phenazon |
16 |
59 |
0,0 |
0,900 |
0,836 |
92,9 |
0,1061 |
12,7 |
0,0229 |
2,7 |
| Primidon |
16 |
61 |
0,0 |
1,162 |
1,106 |
95,2 |
0,1697 |
15,3 |
0,0293 |
2,7 |
| Propyphenazon |
15 |
57 |
6,6 |
0,900 |
0,830 |
92,2 |
0,0796 |
9,6 |
0,0177 |
2,1 |
| Roxithromycin |
15 |
57 |
6,6 |
1,062 |
1,866 |
175,7 |
1,0034 |
53,8 |
0,1143 |
6,1 |
| Sotalol |
16 |
61 |
0,0 |
1,141 |
1,055 |
92,4 |
0,2713 |
25,7 |
0,0352 |
3,3 |
| Sulfamethoxazol |
14 |
52 |
8,8 |
1,104 |
0,969 |
87,8 |
0,1986 |
20,5 |
0,0253 |
2,6 |
| Temazepam |
14 |
53 |
7,0 |
0,900 |
0,786 |
87,3 |
0,1315 |
16,7 |
0,0204 |
2,6 |
| Trimethoprim |
16 |
61 |
0,0 |
0,946 |
0,873 |
92,3 |
0,1680 |
19,3 |
0,0195 |
2,2 |
| CHÚ THÍCH: Giải thích ký hiệu xem trong Bảng A.2 | ||||||||||
Bảng B.1 – Độ thu hồi các mẫu hiệu chuẩn trong quá trình lọc
|
Chất |
A1 |
A2 |
A3 |
A4 |
AiF |
s |
| 4-Axetamidoantipyrin |
100 |
101 |
98 |
99 |
99,5 |
1,3 |
| N-Axetyl sulfamethoxazol |
100 |
93 |
99 |
102 |
98,5 |
3,9 |
| Atenolol |
99 |
101 |
100 |
102 |
100,5 |
1,3 |
| Atorvastatina |
84 |
83 |
87 |
83 |
84,3 |
2,2 |
| Bezafibrat |
98 |
94 |
100 |
100 |
98,0 |
2,9 |
| Bisoprolol |
91 |
92 |
94 |
90 |
91,8 |
1,9 |
| Candesartana |
99 |
98 |
103 |
. 100 |
100,0 |
2,2 |
| Carbamazepin |
103 |
104 |
108 |
102 |
104,3 |
2,5 |
| Clarithromycin |
71 |
74 |
80 |
73 |
74,5 |
5,2 |
| Clenbuterola |
98 |
95 |
100 |
95 |
97,0 |
2,5 |
| Axit clofibric |
97 |
94 |
97 |
95 |
95,8 |
1,6 |
| Codeina |
96 |
101 |
100 |
99 |
99,0 |
2,2 |
| Dehydrato-erythromycin |
64 |
66 |
70 |
62 |
65,5 |
5,2 |
| Desvenlafaxina |
97 |
94 |
96 |
92 |
94,8 |
2,3 |
| Diazepam |
96 |
95 |
97 |
92 |
95,0 |
2,3 |
| Diclofenac |
108 |
101 |
101 |
100 |
102,5 |
3,6 |
| Dihydrocodeina |
99 |
97 |
95 |
94 |
96,3 |
2,3 |
| Dihydro-dihydroxy-carbamazepin |
95 |
97 |
97 |
94 |
95,8 |
1,6 |
| Erythromycin |
80 |
81 |
83 |
80 |
81,0 |
1,7 |
| 4-Formylaminoantipyrin |
100 |
97 |
95 |
93 |
96,3 |
3,1 |
| Axit Fenofibrica |
93 |
91 |
90 |
90 |
91,0 |
1,6 |
| Furosemina |
92 |
95 |
92 |
91 |
92,5 |
1,9 |
| Gabapentina |
99 |
96 |
101 |
98 |
98,5 |
2,1 |
| Gemfibrozil |
90 |
91 |
91 |
91 |
90,8 |
0,6 |
| Ibuprofen |
99 |
97 |
99 |
97 |
98,0 |
1,2 |
| Indometacina |
95 |
97 |
93 |
91 |
94,0 |
2,7 |
| A độ thu hồi (phép đo lặp)b.
AiF độ thu hồi chất i trong quá trình lọc, tính theo phần trăm (%), s độ lệch chuẩn, tinh theo phần trăm (%). a Các chất khác phù hợp với Bảng E.1. b Dữ liệu đã xử lý phù hợp với Điều 10. c Bộ lọc bằng xyranh, có thể tích chết nhỏ, đường kính 13 mm có màng lọc xenlulo tái tạo. |
||||||
Bảng B.1 – (kết thúc)
|
Chất |
A1 |
A2 |
A3 |
A4 |
AiF |
s |
| Losartana |
100 |
105 |
102 |
103 |
102,5 |
2,0 |
| Metformina |
91 |
92 |
89 |
89 |
90,3 |
1,7 |
| Metolprolol |
95 |
101 |
98 |
96 |
97,5 |
2,7 |
| Metronidazola |
103 |
105 |
104 |
104 |
104,0 |
0,8 |
| Moxifloxacina |
84 |
85 |
83 |
82 |
83,5 |
1,5 |
| Nadolola |
96 |
97 |
99 |
100 |
98,0 |
1,9 |
| Naproxen |
94 |
94 |
92 |
92 |
93,0 |
1,2 |
| Oxazepam |
95 |
94 |
91 |
91 |
92,8 |
2,2 |
| Phenazon |
93 |
96 |
99 |
93 |
95,3 |
3,0 |
| Primidon |
102 |
103 |
105 |
96 |
101,5 |
3,8 |
| Propranolola |
107 |
106 |
105 |
104 |
105,5 |
1.2 |
| Propyphenazon |
98 |
97 |
97 |
97 |
97,3 |
0,5 |
| Axit ritalinica |
96 |
102 |
100 |
100 |
99,5 |
2,5 |
| Roxithromycin |
55 |
54 |
54 |
46 |
52,3 |
8,0 |
| Sotalol |
101 |
103 |
104 |
97 |
101,3 |
3,1 |
| Sulfadiazina |
93 |
94 |
96 |
100 |
95,8 |
3,2 |
| Sulfadimethoxina |
105 |
104 |
106 |
103 |
104,5 |
1,2 |
| Sulfadoxina |
90 |
88 |
86 |
87 |
87,8 |
1,9 |
| Sulfamerazina |
96 |
95 |
95 |
92 |
94,5 |
1,8 |
| Sulfamethazina |
96 |
95 |
94 |
93 |
94,5 |
1,4 |
| Sulfamethoxazol |
98 |
95 |
97 |
96 |
96,5 |
1,3 |
| Sulfathiazola |
104 |
101 |
101 |
99 |
101,3 |
2,0 |
| Temazepam |
93 |
96 |
95 |
94 |
94,5 |
1,4 |
| Tramadola |
98 |
100 |
100 |
99 |
99,3 |
1,0 |
| Trimethoprim |
101 |
97 |
103 |
104 |
101,3 |
3,1 |
| Valsartana |
106 |
104 |
107 |
102 |
104,8 |
2,1 |
| Venlafaxina |
96 |
95 |
96 |
94 |
95,3 |
1,0 |
| A độ thu hồi (phép đo lặp)b.
AiF độ thu hồi chất i trong quá trình lọc, tính theo phần trăm (%), s độ lệch chuẩn, tính theo phần trăm (%). a Các chất khác phù hợp với Bảng E.1. b Dữ liệu đã xử lý phù hợp với Điều 10. c Bộ lọc bằng xyranh, có thể tích chết nhỏ, đường kính 13 mm có màng lọc xenlulo tái tạo. |
||||||
Ví dụ về cột HPLC và sắc ký đồ
C.1 Các điều kiện sắc ký thu được sắc ký đồ trong Hình C.1
| Tiền cột/ | Ultra Cartridges C-18 ID 2,1 mm |
| cột tách: | Synergi Hydro-RPa 2,5 μm, 100 mm x 2 mm |
| Bơm: | 100 μL dung dịch chuẩn trong nước uống, ρ = 0,1 μg/L |
| Pha động: | A: axit axetic 0,1 % với amoni axetat 1 mmol trong nước |
| B: axit axetic 0,1 % trong axetonitril | |
| Gradient: | 0 min đến 2 min: 4 % B, đẳng dòng; 2 min đến 20 min: 4 % B đến 75 % B, tuyến tính; |
| 20 min đến 25 min: 95 % B, đẳng dòng; 25 min đến 35 min: 4 % B, đẳng dòng | |
| Tốc độ dòng: | 0,25 mL/min |
| Nhiệt độ cột: | 40 °C |
| Áp suất: | 16 MPa ở điều kiện ban đầu |
a Ultra Cartridges C-18, Synergi Hydro-RP là ví dụ về sản phẩm phù hợp có sẵn. Thông tin này chỉ tạo thuận lợi cho người sử dụng tiêu chuẩn này và không phải là xác nhận của tiêu chuẩn về sản phẩm này.
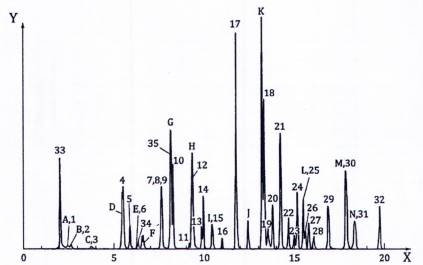
CHÚ DẪN
| X | thời gian, min | E | iopromin-D3 |
| Y | cường độ tín hiệu (ESI dương/âm) | F | sulfadiazin-D4 |
| Đối với pic từ số 1 đến 32, xem Bảng C.1 | G | trimethoprim-D9 | |
| 33 | metformin | H | phenazon-D3 |
| 34 | gabapentin | I | sulfamethoxazol-D4 |
| 35 | axit ritalinic | J | propranolol-D7 |
| A | ipoamidol-D3 | K | carbamazepin-D10 |
| B | axit diatrizoic-D6 | L | Bezafibrat-D4 |
| C | iomeprol-D3 | M | diclofenac-D4 |
| D | sotalol-D6 | N | ibuprofen-D3 |
HÌnh C.1 – Tách sắc ký, ví dụ 1, sắc ký đồ TIC
C.2 Các điều kiện sắc ký thu được sắc ký đồ trong Hình C.2
| Cột tách: | Kinetex EVO C18a 100A (150 X 2,1 mm; 5 μm) |
| Thể tích bơm: | 40 μL |
| Pha động: | A: nước với amoni axetat 1 mmol/L |
| B: metanol với amoni axetat 1 mmol/L | |
| Gradient: | 5 min 98 % A, 20 min 98 % A đến 2% A (tuyến tính) |
| 9 min 2% A, 1 min 2 % A đến 9 8% A, 7 min 98 % A | |
| Tốc độ dòng: | 0,2 mL/min |
| Nhiệt độ cột: | 40 °C |
| Áp suất: | 15 MPa ở điều kiện ban đầu |
a Kinetex EVO C18 là ví dụ về sản phẩm phù hợp có sẵn. Thông tin này chỉ tạo thuận lợi cho người sử dụng tiêu chuẩn này và không phải là xác nhận của tiêu chuẩn về sản phẩm này.
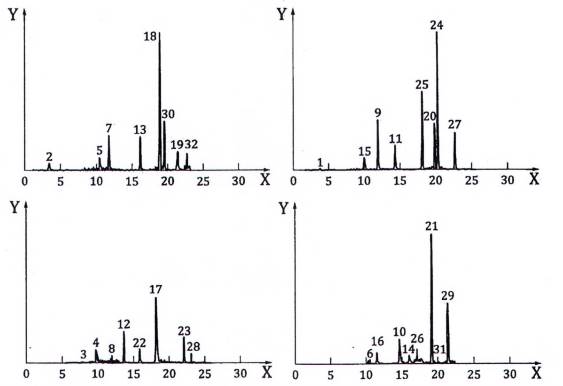
CHÚ DẪN
X thời gian, min
Y cường độ tín hiệu tương đối (ESI dương/âm)
Đối với pic từ số 1 đến 32, xem Bảng C.1
Hình C.2 – Tách sắc ký và cường độ tín hiệu đối với các chuyển khối ở 25 ng/L, ví dụ 2, sắc ký đồ MS/MS
C.3 Các điều kiện sắc ký thu được sắc ký đồ trong Hình C.3
| Cột tách: | ACQUITY UPLC HSS T3a 50 x 2,1 mm, 1,8 μm (vật liệu C18 cải tiến; Nước) |
| Cột làm giàu: | Hypersil Gold C18a, 20 x 2,1 mm, 12 μm |
| Bơm: | 1 mL vào cột làm giàu (1 mL/min, thêm MeOH 1 %) |
| Pha động: | A: nước với MeOH 1 %, axit formic 0,1 % |
| B: metanol với axit formic 0,1 % | |
| Gradient: | 1,3 min 99 % A, 8 min đến 5 % A đến 12 min tuyến tính từ 12 min đến 15 min 99 % A |
| Tốc độ dòng: | 0,6 mL/min |
| Nhiệt độ cột: | 30 °C |
| Áp suất: | 30 MPa ở điều kiện ban đầu |
a ACQUITY UPLC HSS T3, Hypersil Gold C18 là ví dụ về sản phẩm phù hợp có sẵn. Thông tin này chỉ tạo thuận lợi cho người sử dụng tiêu chuẩn này và không phải là xác nhận của tiêu chuẩn về sản phẩm này.
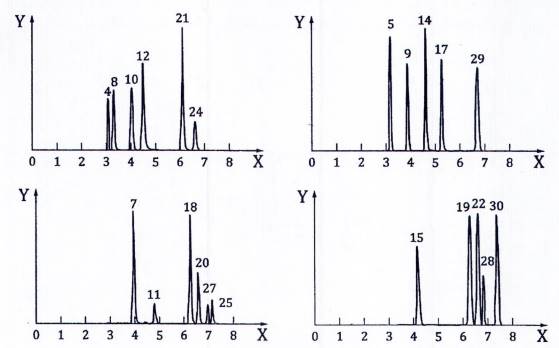
CHÚ DẪN
X thời gian, min
Y cường độ tín hiệu tương đối (ESI dương/âm)
Đối với pic từ số 1 đến 32, xem Bảng C.1.
Hình C.3 – Tách sắc ký và cường độ tín hiệu (độ chính xác khối lượng ± 5 pμm) đối với chuyển khối ở 125 ng/L, ví dụ 3, sắc ký đồ HRMS
C.4 Các điều kiện sắc ký thu được sắc ký đồ trong Hình C.4
| Cột tách: | ACQUITY UPLC HSS T3a 1,8 μm, 100mmx2,1 mm |
| Bơm: | 100 μL dung dịch chuẩn trong nước uống, ρ = 0,1 μg/L |
| Pha động: | A: axit axetic 0,05 % trong nước |
| B: axetonitril | |
| Gradient: | 0 min đến 0,5 min: 2 % B đẳng dòng; 0,5 min đến 7 min: 2% B đến 100 % B, tuyến tính;
7 min đến 9 min: 100 % B đẳng dòng; 9 min đến 11 min: 100% B đến 2 % B, đẳng dòng |
| ibuprofen: 0 min đến 0,5 min: 50 % B đẳng dòng; 0,5 min đến 3,5 min: 50 % B đến 100% B tuyến tính; 3,5 min đến 4,5 min: 100 % B đẳng dòng; 4,5 min đến 6 min: 50 % B, đẳng dòng | |
| Tốc độ dòng: | 0,4 mL/min |
| Nhiệt độ cột: | 40 °C |
| Áp suất: | 50 MPa ở điều kiện ban đầu, ibuprofen: 60 MPa |
a ACQUITY UPLC HSS T3 là ví dụ về sản phẩm phù hợp có sẵn. Thông tin này chỉ tạo thuận lợi cho người sử dụng tiêu chuẩn này và không phải là xác nhận của tiêu chuẩn về sản phẩm này.
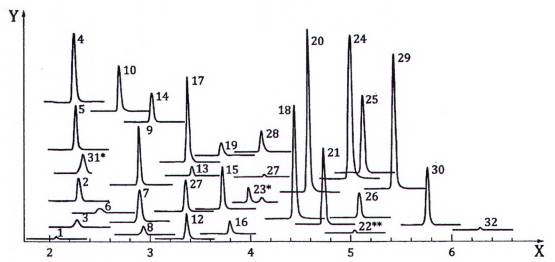
CHÚ DẪN
X thời gian, min
Y cường độ tín hiệu tương đối (ESI dương/âm)
Đối với pic từ số 1 đến 32, xem Bảng C.1.
23* dehydrato-erythromycin
22** axit clofibric (phóng to 100 lần)
31* ibuproten ( phóng to 10 lần)
Hình C.4 – Sắc ký đồ tách, ví dụ 4, sắc đồ MS/MS
Bảng C.1 – Số pic và chi tiết phát hiện biểu thị trên Hình C.1 đến Hình C.4
|
Số pic |
Chất |
Chuyển đổi khối lượng m/z (Hình C.2) |
Khối lượng chiết m/z (Hình C.3) |
|
1 |
lopamidol |
795 > 778 (NH4) |
777,8614 |
|
2 |
Axit diatrizoic |
632 > 361 (NH4) |
631,8000 |
|
3 |
lomeprol |
795 > 405 (NH4) |
777,8614 |
|
4 |
Sotalol |
273 > 133 |
273,1267 |
|
5 |
Atenolol |
267 > 145 |
267,1703 |
|
6 |
lopromin |
809 > 792 (NH4) |
791,8771 |
|
7 |
4-Formylaminoantipyrin |
232 > 83 |
232,1081 |
|
8 |
4-Aminoantipyrina |
204 > 56 |
204,1131 |
|
9 |
4-Axetylamidoantipyrin |
246 > 104 |
246,1237 |
|
10 |
Trimethoprim |
291 > 230 |
291,1452 |
|
11 |
Primidon |
219 > 162 |
219,1128 |
|
12 |
Phenazon |
189 > 56 |
189,1022 |
|
13 |
10,11-Dihydro-10,11-dihydroxy carbamazepin |
271 > 180 |
271,1077 |
|
14 |
Metoprolol |
268 > 77 |
268,1907 |
|
15 |
Sulfamethoxazol |
254 > 156 |
254,0594 |
|
16 |
N4-Axetyl sulfamethoxazol |
296 > 134 |
296,0700 |
|
17 |
Bisoprolol |
326 > 116 |
326,2326 |
|
18 |
Carbamazepin |
237 > 194 |
237,1022 |
|
19 |
Erythromycin |
734 > 158 |
734,4685 |
|
20 |
Oxazepam |
287 > 241 |
287,0582 |
|
21 |
Propyphenazon |
231 > 189 |
231,1492 |
|
22 |
Axit clofibric |
213 > 127 |
213,0324 |
|
23 |
Dehydrato-Erythromycin |
716 > 158 |
716,4580 |
|
24 |
Temazepam |
301 > 255 |
301,0738 |
|
25 |
Bezafibrat |
362 > 139 |
362,1154 |
|
26 |
Naproxen |
231 > 115 |
231,1016 |
|
27 |
Clarithromycin |
748 > 158 |
748,4842 |
|
28 |
Roxithromycin |
838 > 680 |
837,5319 |
|
29 |
Diazepam |
285 > 193 |
285,0789 |
|
30 |
Diclofenac |
296 > 214 |
296,0240 |
|
31 |
Ibuprofen |
205 > 159 |
205,1234 |
|
32 |
Gemfibrozil |
268 > 129 (NH4) |
249,1496 |
| a không phải là một phần của xác nhận giá trị sử dụng. | |||
Bảng D.1 – Các chuyển khối (MS/MS) của các chất phù hợp với Bảng 1
|
Chất |
ion hóa |
ion mẹ 1 m/z |
ion sản phẩm m/z |
ion mẹ 2 m/z |
ion sản phẩm m/z |
||||
| 4-Axetylaminoantipyrin |
ESI dương |
246 |
228 |
104 |
83 |
|
|
|
|
| N4-Axetyl sulfamethoxazol |
ESI dương |
296 |
198 |
134 |
108 |
65 |
|
|
|
| N4-Axetyl sulfamethoxazol |
ESI âm |
294 |
198 |
134 |
|
|
|
|
|
| Axit diatrizoic |
ESI dương |
615 |
361 |
233 |
|
|
632 |
361 |
233 |
| Atenolol |
ESI dương |
267 |
145 |
190 |
74 |
56 |
|
|
|
| Bezafibrat |
ESI dương |
362 |
316 |
139 |
121 |
|
|
|
|
| Bezafibrat |
ESI âm |
360 |
274 |
154 |
|
|
|
|
|
| Bisoprolol |
ESI dương |
326 |
116 |
107 |
74 |
|
|
|
|
| Carbamazepin |
ESI dương |
237 |
194 |
192 |
179 |
|
|
|
|
| Clarithromycin |
ESI dương |
748 |
590 |
158 |
83 |
|
|
|
|
| Axit clofibric |
ESI âm |
213 |
127 |
85 |
|
|
215 |
129 |
|
| Dehydrato-Erythromycin |
ESI dương |
716 |
558 |
158 |
116 |
|
|
|
|
| Diazepam |
ESI dương |
285 |
193 |
154 |
222 |
|
|
|
|
| Diclofenac |
ESI dương |
296 |
250 |
214 |
215 |
|
298 |
214 |
216 |
| Diclofenac |
ESI âm |
294 |
250 |
214 |
|
|
296 |
252 |
|
| 10,11 -Dihydro-10,11 -dihydroxy carbamazepin |
ESI dương |
271 |
236 |
210 |
180 |
|
|
|
|
| Erythromycin |
ESI dương |
734 |
576 |
158 |
83 |
|
|
|
|
| 4-Formylaminoantipyrin |
ESI dương |
232 |
204 |
104 |
83 |
56 |
|
|
|
| Gemfibrozil |
ESI âm |
249 |
127 |
121 |
106 |
83 |
|
|
|
| Ibuprofen |
ESI âm |
205 |
161 |
159 |
|
|
|
|
|
| lomeprol |
ESI dương |
778 |
687 |
559 |
532 |
405 |
795 |
686 |
|
| lopamidol |
ESI dương |
778 |
687 |
559 |
542 |
387 |
795 |
559 |
|
| lopromin |
ESI dương |
792 |
573 |
559 |
300 |
|
809 |
792 |
|
| Metoprolol |
ESI dương |
268 |
133 |
131 |
116 |
77 |
|
|
|
| Naproxen |
ESI âm |
229 |
185 |
169 |
170 |
|
231 |
185 |
115 |
| Oxazepam |
ESI dương |
287 |
269 |
241 |
104 |
|
|
|
|
| Phenazon |
ESI dương |
189 |
104 |
77 |
56 |
|
|
|
|
| Primidon |
ESI dương |
219 |
162 |
119 |
91 |
|
|
|
|
| Propyphenazon |
ESI dương |
231 |
201 |
189 |
146 |
56 |
|
|
|
| Roxithromycin |
ESI dương |
838 |
680 |
158 |
|
|
|
|
|
| Sotalol |
ESI dương |
273 |
255 |
213 |
133 |
|
|
|
|
| Sulfamethoxazol |
ESI dương |
254 |
156 |
108 |
92 |
|
|
|
|
| Temazepam |
ESI dương |
301 |
283 |
255 |
193 |
177 |
|
|
|
| Trimethoprim |
ESI dương |
291 |
261 |
230 |
123 |
|
|
|
|
Các giá trị m/z tối ưu có thể sai lệch so với các giá trị cho trong bảng và do đó phải được xác định riêng lẻ trong điều kiện sắc ký, nếu có thể. Nếu sử dụng các đệm có chứa amoni, thì các sản phẩm cộng amoni ([M+NH4)+] có thể tạo ra tín hiệu mạnh hơn đối với một số chất phân tích so với các ion phân tử [M+H]+).
Bảng D.2 – Các chuyển khối (MS/HRMS) của các chất phù hợp với Bảng 1
|
Chất |
ion hóa |
Khối lượng đồng vị monoa U |
ion mẹb m/z |
ion sản phẩm 1b m/z |
ion sản phẩm 2b m/z |
ion sản phẩm 3b m/z |
| 4-Axetylaminoantipyrin |
ESI dương |
245,1164 |
246,1237 |
228,1130 |
204,1127 |
159,0920 |
| N4-Axetyl sulfamethoxazol |
ESI dương |
295,0626 |
296,0700 |
134,0592 |
108,0437 |
65,0386 |
| Axit diatrizoic |
ESI dương |
613,7696 |
614,7769 631,8000 |
360,9681 |
233,0571 |
318,9581 |
| Atenolol |
ESI dương |
266,1630 |
267,1703 |
145,0637 |
133,0637 |
164,0689 |
| Bezafibrat |
ESI dương |
361,1080 |
362,1154 |
138,9936 |
121,0642 |
161,0943 |
| Bisoprolol |
ESI dương |
325,2253 |
326,2326 |
116,103 |
133,0629 |
147,0784 |
| Carbamazepin |
ESI dương |
236,0949 |
237,1022 |
194,0957 |
192,0798 |
193,0877 |
| Clarithromycin |
ESI dương |
747,4768 |
748,4842 |
158,1168 |
590,3928 |
83,0489 |
| Axit clofibric |
ESI âm |
214,0396 |
213,0324 |
126,9953 |
– |
– |
| Dehydrato-Erythromycin |
ESI dương |
715,4506 |
716,4580 |
158,1163 |
– |
– |
| Diazepam |
ESI dương |
284,0716 |
285,0789 |
193,0872 |
222,1132 |
154,0419 |
| Diclofenac |
ESI dương |
295,0166 |
296,0240 |
214,0408 |
215,0487 |
250,0167 |
| 10,11-Dihydro-10,11- dihydroxy carbamazepin |
ESI dương |
270,1004 |
271,10772 |
180,0807 |
182,0952 |
210,0896 |
| Erythromycin |
ESI dương |
733,4612 |
734,4685 |
576,3753 |
558,3647 |
522,3439 |
| 4-Formylaminoantipyrin |
ESI dương |
231,1007 |
232,1081 |
214,0964 |
204,1120 |
187,0855 |
| Gemfibrozil |
ESI âm |
250,1568 |
249,1496 |
121,0658 |
45,0000 |
– |
| Ibuprofen |
ESI âm |
206,1306 |
205,1234 |
161,0987 |
– |
– |
| lomeprol |
ESI dương |
776,8541 |
777,8614 |
404,9946 |
531,8947 |
331,9436 |
| lopamidol |
ESI dương |
776,8541 |
777,8614 |
558,8809 |
541,8839 |
531,8995 |
| lopromin |
ESI dương |
790,8697 |
791,8771 |
572,9087 |
558,8861 |
527,8692 |
| Metoprolol |
ESI dương |
267,1834 |
268,1907 |
191,1055 |
159,0800 |
133,0650 |
| Naproxen |
ESI dương |
230,0942 |
231,1016 |
185,0943 |
170,0716 |
153,0693 |
| Oxazepam |
ESI dương |
286,0509 |
287,0582 |
269,0480 |
241,0524 |
231,0636 |
| Phenazon |
ESI dương |
188,0949 |
189,1022 |
147,0905 |
130,0643 |
144,0797 |
| Primidon |
ESI dương |
218,1055 |
219,1128 |
162,0914 |
117,0694 |
134,0952 |
| Propyphenazon |
ESI dương |
230,1419 |
231,1492 |
189,1016 |
201,1009 |
56,0507 |
| Roxithromycin |
ESI dương |
836,5245 |
837,5319 |
679,4407 |
158,1175 |
|
| Sotalol |
ESI dương |
272,1194 |
273,1267 |
133,0752 |
134,0824 |
106,0649 |
| Sulfamethoxazol |
ESI dương |
253,0521 |
254,0594 |
156,0106 |
160,0855 |
147,0779 |
| Temazepam |
ESI dương |
300,0665 |
301,0738 |
255,0683 |
|
|
| Trimethoprim |
ESI dương |
290,1378 |
291,1452 |
230,1162 |
261,0967 |
275,1119 |
| a tính sử dụng công thức phân tử.
b đo. |
||||||
Bảng D.3 – Các chuyển khối của các chất chuẩn nội thích hợp
|
Chất |
Khối lượng đồng vị mono u |
ion mẹ m/z |
ion sản phẩm m/z |
| 4-Axetylaminoantipyrin-D3 |
248,1353 |
249 |
231 |
| Axit diatrizoic-D6 |
619,8073 |
621 |
367 |
| Atenolol-D7 |
273,2069 |
274 |
145 |
| Bezafibrat-D4 |
365,1331 |
366 |
143 |
| Bisoprolol-D5 |
330,2567 |
331 |
121 |
| Carbamazepin-D10 |
246,1577 |
247 |
204 |
| Diazepam-D5 |
330,2567 |
290 |
198 |
| Diclofenac-D4 |
299,0417 |
300 |
218 |
| lbuprofen-D3 |
209,1495 |
208 |
164 |
| lomeprol-D3 |
779,8730 |
781 |
408 |
| lopamidol-D3 |
779,8730 |
781 |
562 |
| lopromin-D3 |
793,8886 |
795 |
576 |
| Metoprolol-D7 |
274,2380 |
275 |
143 |
| Oxazepam-D5 |
291,0823 |
292 |
241 |
| Phenazon-D3 |
191,1137 |
192 |
59 |
| Primidon-D5 |
223,1369 |
224 |
167 |
| Sotalol-D6 |
278,1571 |
279 |
134 |
| Sulfamethoxazol-D4 |
257,0772 |
258 |
160 |
| Trimethoprim-D9 |
299,1943 |
300 |
234 |
Ví dụ về phần mở rộng của phương pháp
Bảng E.1 – Chuyển khối của các chất khác
|
Chất |
Khối lượng đồng vị mono u |
ion mẹ m/z |
ion sản phẩm m/z |
|
| Atorvastatin |
558,2530 |
559 |
440 |
250 |
| Candesartan |
440,1597 |
441 |
263 |
423 |
| Clenbuterol |
276,0796 |
277 |
203 |
132 |
| Codein |
299,1521 |
300 |
152 |
115 |
| Desvenlafaxin |
263,1885 |
264 |
246 |
107 |
| Dihydrocodein |
301,1678 |
302 |
199 |
128 |
| Eprosartan |
424,1457 |
425 |
107 |
207 |
| Axit fenofibric |
318,0659 |
317 |
231 |
|
| Furosemin |
330,0077 |
329 |
285 |
205 |
| Gabapentin |
171,1259 |
172 |
137 |
95 |
| Indometacin |
357,0768 |
358 |
139 |
111 |
| Irbesartan |
428,2325 |
429 |
207 |
180 |
| Losartan |
422,1622 |
421 |
127 |
179 |
| Metformin |
129,1015 |
130 |
60 |
71 |
| Metronidazol |
171,0644 |
172 |
128 |
82 |
| Moxifloxacin |
401,1751 |
402 |
384 |
358 |
| Nadolol |
309,1940 |
310 |
254 |
201 |
| Propranolol |
259,1572 |
260 |
116 |
183 |
| Axit ritalinic |
219,1259 |
220 |
84 |
56 |
| Sulfadiazin |
250,0525 |
251 |
156 |
92 |
| Sulfadimethoxin |
310,0736 |
311 |
156 |
92 |
| Sulfadoxin |
310,0736 |
311 |
156 |
92 |
| Sulfamerazin |
264,0681 |
265 |
156 |
92 |
| Sulfamethazin |
278,0838. |
279 |
186 |
124 |
| Sulfathiazol |
255,0136 |
256 |
92 |
108 |
| Telmisartan |
514,2369 |
515 |
276 |
497 |
| Tramadol |
263,1885 |
264 |
58 |
|
| Valsartan |
435,2270 |
436 |
207 |
235 |
| Venlafaxin |
277,2042 |
278 |
121 |
91 |
Thư mục tài liệu tham khảo
[1] ISO 11352, Water quality – Estimation of measurement uncertainty based on validation and quality control data.
[2] TCVN 6910-2 (ISO 5725-2), Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo – Phần 2: Phương pháp cơ bản xác định độ lặp lại và độ tái lập của phương pháp đo tiêu chuẩn.
Mục lục
Lời nói đầu
Lời giới thiệu
1 Phạm vi áp dụng
2 Tài liệu viện dẫn
3 Thuật ngữ và định nghĩa
4 Nguyên tắc
5 Cản trở
5.1 Trong quá trình chuẩn bị mẫu
5.2 Trong quá trình chạy sắc ký lỏng hiệu năng cao – khối phổ
6 Thuốc thử
6.1 Yêu cầu chung
6.2 Chuẩn bị các dung dịch
7 Thiết bị, dụng cụ
8 Lấy mẫu
9 Cách tiến hành
9.1 Yêu cầu chung
9.2 Chuẩn bị mẫu
9.3 Sắc ký lòng hiệu năng cao (HPLC)
9.4 Phát hiện
9.5 Đo giá trị mẫu trắng
10 Hiệu chuẩn
10.1 Yêu cầu chung
10.2 Hiệu chuẩn bằng chất chuẩn ngoại
10.3 Hiệu chuẩn bằng chất chuẩn nội
11 Tính độ thu hồi
11.1 Yêu cầu chung
11.2 Tính độ thu hồi chất phân tích sử dụng mẫu
11.3 Độ thu hồi chất chuẩn nội
12 Đánh giá
12.1 Kiểm tra xác nhận các chất riêng rẽ
12.2 Tính kết quả riêng rẽ sử dụng hiệu chuẩn với chất chuẩn ngoại
12.3 Tính các kết quả riêng lẻ sử dụng hiệu chuẩn với chất chuẩn nội.
13 Biểu thị kết quả
14 Báo cáo thử nghiệm
Phụ lục A (tham khảo) Dữ liệu hiệu năng
Phụ lục B (tham khảo) Các ví dụ về độ thu hồi
Phụ lục C (tham khảo) Ví dụ về cột HPLC và sắc ký đồ
Phụ lục D (tham khảo) Ví dụ về phát hiện
Phụ lục E (tham khảo) Ví dụ về phần mở rộng của phương pháp
Thư mục tài liệu tham khảo
1) phần triệu (ppm) là đơn vị không còn được sử dụng. Tức là không được chấp nhận bởi hệ thống đơn vị quốc tế SI.
| TIÊU CHUẨN QUỐC GIA TCVN 13676:2023 (ISO 21676:2018) VỀ CHẤT LƯỢNG NƯỚC – XÁC ĐỊNH PHẦN HÒA TAN CỦA MỘT SỐ THÀNH PHẦN DƯỢC HOẠT TÍNH, SẢN PHẨM CHUYỂN HÓA VÀ CÁC CHẤT HỮU CƠ KHÁC TRONG NƯỚC VÀ NƯỚC THẢI ĐÃ QUA XỬ LÝ – PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO – KHỐI PHỔ (HPLC-MS/MS HOẶC -HRMS) SAU KHI BƠM TRỰC TIẾP | |||
| Số, ký hiệu văn bản | TCVN13676:2023 | Ngày hiệu lực | |
| Loại văn bản | Tiêu chuẩn Việt Nam | Ngày đăng công báo | |
| Lĩnh vực |
Tài nguyên - môi trường |
Ngày ban hành | |
| Cơ quan ban hành | Tình trạng | Còn hiệu lực | |
Các văn bản liên kết
| Văn bản được hướng dẫn | Văn bản hướng dẫn | ||
| Văn bản được hợp nhất | Văn bản hợp nhất | ||
| Văn bản bị sửa đổi, bổ sung | Văn bản sửa đổi, bổ sung | ||
| Văn bản bị đính chính | Văn bản đính chính | ||
| Văn bản bị thay thế | Văn bản thay thế | ||
| Văn bản được dẫn chiếu | Văn bản căn cứ |